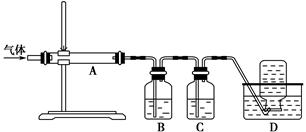
题目内容
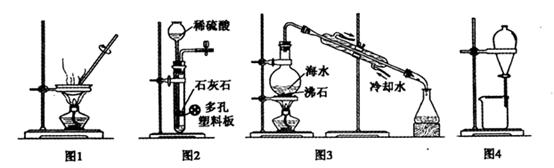
下列实验操作中错误的是
| A.过滤操作时如果有必要可以用蒸馏水洗涤滤纸上的沉淀2-3次 |
| B.蒸馏操作时,应使温度计水银球插入液态混合物中 |
| C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D.萃取操作时,要不断振摇分液漏斗并放气 |
B
试题分析:A、正确;B、蒸馏时,温度计测量的是蒸汽的温度,应与蒸馏烧瓶的支管口下端相平,错误;C、正确;D、萃取时,为了充分萃取要震摇,震摇时产生气泡,所以要放气,正确。

练习册系列答案
相关题目

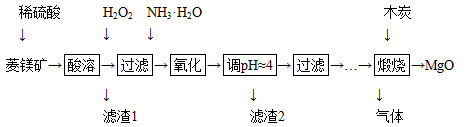
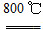 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑