题目内容
下列说法正确的是( )
| A、向饱和Na2CO3溶液中通入足量的CO2,溶液变浑浊,由此证明了NaHCO3溶解度比Na2CO3小 | ||
| B、C(s,石墨)=C(s,金刚石) 该反应吸热熵减,常压下,升温或者降温均为非自发反应 | ||
| C、在铁制品表面镀锌或者镀锡,都是采用外加保护层的方法来防止铁的腐蚀 | ||
D、向0.1mol/L CH3COOH溶液中加入少量的冰醋酸,溶液中
|
考点:钠的重要化合物,金属的电化学腐蚀与防护,焓变和熵变,弱电解质在水溶液中的电离平衡
专题:
分析:A.向饱和碳酸钠溶液中通入足量的CO2气体时,发生反应:Na2CO3+H2O+CO2=2NaHCO3,由于碳酸氢钠溶解度小于碳酸钠、生成碳酸氢钠质量大于碳酸钠、反应中消耗了水这三个因素,使碳酸氢钠析出;
B.反应能否自发进行取决于△H-T△S是否小于0;
C.锌、锡在空气中氧化生成一层致密氧化膜使其内部不再氧化,从而不易生锈;
D.
=
=
=
,Kw与K(CH3COOH)只受温度影响.
B.反应能否自发进行取决于△H-T△S是否小于0;
C.锌、锡在空气中氧化生成一层致密氧化膜使其内部不再氧化,从而不易生锈;
D.
| C(CH3COO-) |
| C(OH-) |
| C(CH3COO-) | ||
|
| C(CH3COO-)C(H+) |
| Kw |
| K(CH3COOH) |
| Kw |
解答:
解:A.向饱和Na2CO3溶液中通入足量的CO2,溶液变浑浊,发生反应:Na2CO3+H2O+CO2=2NaHCO3,由于碳酸氢钠溶解度小于碳酸钠、生成碳酸氢钠质量大于碳酸钠、反应中消耗了水这三个因素,使碳酸氢钠析出,故A错误;
B.C(s,石墨)=C(s,金刚石)该反应吸热熵减,则△H>0,△S<0,△H-T△S一定大于0,所以该反应一定不能自发进行,故B正确;
C.在铁制品表面镀锌或者镀锡,在空气中氧化生成一层致密氧化膜使其内部不再氧化,从而不易生锈,保护铁不被腐蚀,故C正确;
D.
=
=
=
,Kw与K(CH3COOH)只受温度影响,温度不变,Kw与K(CH3COOH)不变,
不变故D错误;
故选:BC.
B.C(s,石墨)=C(s,金刚石)该反应吸热熵减,则△H>0,△S<0,△H-T△S一定大于0,所以该反应一定不能自发进行,故B正确;
C.在铁制品表面镀锌或者镀锡,在空气中氧化生成一层致密氧化膜使其内部不再氧化,从而不易生锈,保护铁不被腐蚀,故C正确;
D.
| C(CH3COO-) |
| C(OH-) |
| C(CH3COO-) | ||
|
| C(CH3COO-)C(H+) |
| Kw |
| K(CH3COOH) |
| Kw |
| C(CH3COO-) |
| C(OH-) |
故选:BC.
点评:本题为综合题,考查了反应自发进行的判断依据、金属的腐蚀与防护、弱电解质的电离,题目难度比较大,明确反应进行判断依据、弱电解质电离的规律是解题关键,注意BD为易错选项.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
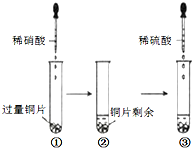 某实验过程如图所示,则图③试管中的现象是( )
某实验过程如图所示,则图③试管中的现象是( )| A、铜片溶解,产生无色气体,该气体遇空气变为红棕色 |
| B、铜片溶解,产生无色气体,该气体遇到空气不变色 |
| C、铜片溶解,放出红棕色有刺激性气味的气体 |
| D、无明显现象,因稀硫酸不与铜反应 |
羧酸和醇反应生成酯的相对分子质量为90,该反应的反应物是( )
A、 和CH3CH2OH 和CH3CH2OH |
B、 和CH3CH2-18OH 和CH3CH2-18OH |
C、 和CH3CH2-18OH 和CH3CH2-18OH |
D、 和CH3CH2OH 和CH3CH2OH |
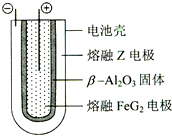 有X、Y、Z、M、G五种元素,是分属三个短周期并且原子序数依次增大的主族元素.其中X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子.完成下列填空:
有X、Y、Z、M、G五种元素,是分属三个短周期并且原子序数依次增大的主族元素.其中X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子.完成下列填空: