题目内容
已知:①2CO(g)+O2(g)=2CO2(g)△H=-568kJ/mol②H2(g)+
O2(g)=H2O(g)△H=-248kJ/mol
已知CO和H2的混合物2.5mol在氧气中充分燃烧放出的热量680kJ,则该混合气体中CO和氢气的物质的量的比值为( )
| 1 |
| 2 |
已知CO和H2的混合物2.5mol在氧气中充分燃烧放出的热量680kJ,则该混合气体中CO和氢气的物质的量的比值为( )
| A、1:1 | B、2:1 |
| C、3:1 | D、3:2 |
考点:有关反应热的计算
专题:计算题
分析:设出CO和H2的物质的量,根据两者的物质的量共为2.5mol,和在氧气中充分燃烧放出的热量为680kJ,列方程组计算即可.
解答:
解:根据题目分析可知,设CO的物质的量为X,H2的物质的量为Y.
由CO和H2的混合物为2.5mol,可得:X+Y=2.5 ①
由CO和H2在氧气中充分燃烧放出的热量680kJ,可得:X×
+Y×248=680 ②
解①②得:X=1.66、Y=0.83,
故该混合气体中CO和氢气的物质的量的比值为2:1,
故选B.
由CO和H2的混合物为2.5mol,可得:X+Y=2.5 ①
由CO和H2在氧气中充分燃烧放出的热量680kJ,可得:X×
| 568 |
| 2 |
解①②得:X=1.66、Y=0.83,
故该混合气体中CO和氢气的物质的量的比值为2:1,
故选B.
点评:本题考查了反应热的有关计算,解题时应注意2molCO燃烧放出568KJ的热量,即1mol放出284KJ的热量.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案
相关题目
下列叙述正确的是( )
| A、乙烯的最简式C2H4 |
| B、乙醇的结构简式C2H6O |
C、四氯化碳的电子式 |
| D、碳原子以四对共用电子对与其它原子的结合 |
自来水可以用氯气消毒.某学生用自来水配制下列物质的溶液,不会产生明显药品变质的是( )
| A、石蕊 |
| B、AgNO3 |
| C、NaHCO3 |
| D、FeCl3 |
五种短周期元素的某些性质如下表所示:
下列说法正确的是( )
| 元素代号 | X | W | Y | Z | Q |
| 原子半径(×10-12m) | 37 | 99 | 66 | 104 | 154 |
| 主要化合价 | +1 | -1、+7 | -2 | -2、+6 | +1 |
| A、由Q与Y形成的化合物中只存在离子键 |
| B、Z与X之间形成的化合物具有还原性 |
| C、X、Y元素组成的化合物的沸点高于X、Z元素组成化合物的沸点是由于Y非金属性比Z强 |
| D、Y、Q、W三种元素组成化合物的水溶液一定显碱性 |
关于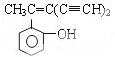 ,下列说法正确的是( )
,下列说法正确的是( )
 ,下列说法正确的是( )
,下列说法正确的是( )| A、一定在同一平面的碳原子有9个 |
| B、一定在同一平面的碳原子有7个 |
| C、1mol此物质与浓溴水混和最多消耗5mol溴 |
| D、可使KMnO4溶液褪色,是苯酚的同系物 |
化学在生产和日常生活中有着重要的应用.下列叙述正确的是( )
| A、汽车尾气中含有氮的氧化物,是汽油不完全燃烧造成的 |
| B、“辽宁舰”上用于舰载机降落拦阻索的特种钢缆,属于新型无机非金属材料 |
| C、白酒中混有少量塑化剂,少量饮用对人体无害,可以用过滤的方法除去 |
| D、高纯度的二氧化硅用于制作光导纤维,光导纤维遇强碱溶液会“断路” |
下列实验基本操作正确的是( )
| A、用酸式滴定管量取25.10mL的Na2CO3溶液 |
| B、中和滴定时,滴定管洗净后经蒸馏水润洗,即注入标准溶液进行滴定 |
| C、测定溶液pH时,将pH试纸放在表面皿上,用玻璃棒蘸取待测液点到pH试纸中央 |
| D、配制FeCl3饱和溶液时,将FeCl3固体加入沸水中以加速溶解 |
 25℃时,pH均为3的盐酸和醋酸溶液分别加水稀释(忽略温度变化),其pH随溶液体积变化的曲线如图所示.下列说法正确的是( )
25℃时,pH均为3的盐酸和醋酸溶液分别加水稀释(忽略温度变化),其pH随溶液体积变化的曲线如图所示.下列说法正确的是( )| A、Ⅱ是盐酸稀释时的pH变化曲线 | ||
B、醋酸溶液稀释过程中,
| ||
| C、a、b、c三点溶液中水的电离程度由大到小的顺序是a>b>c | ||
| D、用NaOH溶液中和等体积的两种酸溶液,盐酸消耗的NaOH溶液体积多 |