题目内容
11.a、b、c、d均为短周期元素,它们原子的最外层电子数分别为1、3、6、7.a、d的简单离子的电子层结构相同,b、c原子的次外层电子数均为8.下列说法正确的是( )| A. | 氢化物的沸点:c>d | |
| B. | a、b、d的最高价氧化物对应的水化物两两皆能反应 | |
| C. | a、b、c的简单离子都会破坏水的电离平衡 | |
| D. | 简单离子的半径:c>d>a>b |
分析 a、b、c、d均为短周期元素,它们原子的最外层电子数分别为1、3、6、7.b、c原子的次外层电子数均为8,则b为Al、c为S,a、d的简单离子的电子层结构相同,则a为Na、d为F.
A、非金属性:S<F,氟化氢分子间存在氢键;
B、氟元素没有最高价氧化物对应的水化物;
C、a、b、c简单离子分别为Na+、Al3+、S2-,Na+不水解,不破坏水的电离平衡;
D、电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多离子半径越大.
解答 解:A、非金属性:S<F,氟化氢分子间存在氢键,所以化物的沸点:c<d,故A错误;
B、氟元素没有最高价氧化物对应的水化物,故B错误;
C、a、b、c简单离子分别为Na+、Al3+、S2-,Al3+、S2-均水解,破坏水的电离平衡,但Na+不水解,不破坏水的电离平衡,故C错误;
D、电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多离子半径越大,故离子半径c(S2-)>d(F-)>a(Na+)>b(Al3+),故D正确;
故选D.
点评 本题考查结构性质位置关系应用,关键是根据核外电子排布推断与水,熟练掌握元素化合物性质.

练习册系列答案
相关题目
1.氮的固定是几百年来科学家一直研究的课题.
(1)下表列举了不同温度下大气固氮和工业固氮的部分K值.
①分析数据可知:大气固氮反应属于吸热(填“吸热”或“放热”)反应
②分析数据可知:人类不适合大规模模拟大气固氮原因K值小,正向进行的程度小(或转化率低),不适合大规模生产
③从平衡角度考虑.工业固氮应该选择常温条件,但实际工业产生却选择500℃左右的高温,解释其原因从反应速率角度考虑,高温更好,但从催化剂活性等综合因素考虑选择500℃左右合适
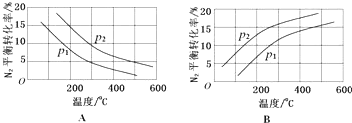
(2)工业固氮反应中,在其他条件相同时,分别测定N2的平衡转化率在不同压强(р1、р2)下随温度变化的曲线,如图所示的图示中,正确的是A(填“A”或“B”);比较р1、р2的大小关系р2>р1.
(3)近年,又有科学家提出在常温、常压、催化剂等条件下合成氨气的新思路,反应原理为:2N2(g)+6H2O(1)?4NH3(g)+3O2(g),则其反应热△H=+1530 kJ•mol-1.
已知:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1
2H2(g)+O2(g)?2H2O(l)△H=-571.6kJ•mol-1.
(1)下表列举了不同温度下大气固氮和工业固氮的部分K值.
| 反应 | 大气固氮 N2(g)+O2(g)?2NO(g) | 工业固氮 N2(g)+3H2(g)?2NH3(g) | |||
| 温度/℃ | 27 | 2000 | 25 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×108 | 0.507 | 0.152 |
②分析数据可知:人类不适合大规模模拟大气固氮原因K值小,正向进行的程度小(或转化率低),不适合大规模生产
③从平衡角度考虑.工业固氮应该选择常温条件,但实际工业产生却选择500℃左右的高温,解释其原因从反应速率角度考虑,高温更好,但从催化剂活性等综合因素考虑选择500℃左右合适
(2)工业固氮反应中,在其他条件相同时,分别测定N2的平衡转化率在不同压强(р1、р2)下随温度变化的曲线,如图所示的图示中,正确的是A(填“A”或“B”);比较р1、р2的大小关系р2>р1.

(3)近年,又有科学家提出在常温、常压、催化剂等条件下合成氨气的新思路,反应原理为:2N2(g)+6H2O(1)?4NH3(g)+3O2(g),则其反应热△H=+1530 kJ•mol-1.
已知:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1
2H2(g)+O2(g)?2H2O(l)△H=-571.6kJ•mol-1.
2.X、Y、Z、W、Q是五种原子序数依次增大的短周期元素,除Z外的另外四种元素在周期表中的位置如图所示,其中Y、W、Q的最高价氧化物对应的水化物与Z的最高价氧化物对应的水化物间均能发生反应,下列说法中正确的是( )
| X | Y | ||
| W | Q |
| A. | 简单离子半径大小关系为:W>Z>Y | |
| B. | 核外最外层电子数:Q>Y>X>W>Z | |
| C. | X与氢元素形成的化合物中,只含极性键 | |
| D. | 常见单质的熔沸点:X>W>Z |
19.X、Y、Z均为短周期元素,原子序数依次增大,X3+比Z2-少一个电子层.以下说法不正确的是( )
| A. | 原子半径:X>Y>Z | B. | 氧化物的熔点:Z>X | ||
| C. | 简单氢化物稳定性:Z>Y | D. | X、Y、Z单质的晶体类型可能有三种 |
6.短周期元素X、Y、Z、Q、T的原子序数与其常见化合价关系如图.下列说法正确的是( )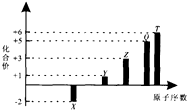

| A. | 1 mol TX2与足量X2反应生成TX3的分子数目为NA | |
| B. | Z元素形成的可溶性盐溶液可能显碱性 | |
| C. | 1 mol Y2X2与足量H2O反应转移的电子数目为2NA | |
| D. | 0.1 molQ元素的含氧酸在水中电离出的H十数目为3NA |
16.某有机物的结构简式如图所示,下列有关该有机物的说法正确的是( )


| A. | 分子中含有四种官能团 | |
| B. | 1mol该有机物完全燃烧消耗O2的物质的量为10mol | |
| C. | 能发生加成、取代、消去、水解等反应 | |
| D. | 相同条件下,等量的该有机物分别与足量的Na和NaHCO3溶液反应产生的气体的量相同 |
3.化学与人类的生活、生产息息相关,下列说法正确的是( )
| A. | BaSO4在医学上用作“钡餐”,Ba2+对人体无害 | |
| B. | 高锰酸钾溶液、酒精、双氧水都能杀菌消毒,消毒原理相同,都利用了强氧化性 | |
| C. | 光导纤维的主要成分是单质硅,太阳能电池使用的材料是SiO2 | |
| D. | “地沟油”禁止食用,但可以用来制肥皂或燃油 |
20.下列说法中不正确的是( )
| A. | 宇宙星体、地球内部都处于高压状态,探究“高压下钠和锂单质金属→绝缘体转变”现象的本质、理解处于高压状态下一些物质的行为具有重要意义,它们可以为研究星体和地球内部构造提供理论支持 | |
| B. | 工业、农业以及日常生活中产生的污水应当分开处理.常用的污水处理方法有中和法、氧化还原法、离子交换法、萃取法、吹脱法、吸附法、电渗析法等,其中前三种属于化学处理方法 | |
| C. | 新型炸药--C4塑胶炸药得名于其空间网状延展结构的每个结构基元含有4个碳原子,由于该炸药成体时无需包裹金属外壳及添加金属芯件,因此能轻易躲过普通X光安全检查,具有较强的隐蔽性 | |
| D. | 建筑领域常使用的黏土、石英、白垩石和多用于农业和食品工业的硅藻土、硅胶均不属于硅酸盐材料的范畴 |
1.烷烃的系统命名法是我国化学学会根据IUPAC并结合我国汉字使用习惯而制定的,其规定必然遵循我们的认知习惯.包括从选主链定“主基调”,给支键编号定坐标,不同基,从简到繁等.这样易辨易写,边读边辨. 在系统命名法中,下列碳原子主链名称不是丁烷的是( )
| A. | (CH3)2CHCH2CH2CH3 | B. | (CH3CH2)2CHCH3 | C. | (CH3)2CHCH(CH3)2 | D. | (CH3)3CCH2CH3 |