题目内容
下列叙述正确的是
A.用锡焊接的铁质器件,焊接处易生锈
B.向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO
C.向饱和FeCl3溶液中滴加过量氨水,可制取Fe(OH)3胶体
D.将钝化后的铝条放入CuSO4溶液中无现象,说明铝的金属性弱于铜
A
【解析】
试题分析:A、用锡焊接的铁质器件,锡、铁和电解质溶液构成原电池,铁作负极发生氧化反应,焊接处易生锈,正确;B、向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,发生的反应为Cl2 +2FeCl2 ====2FeCl3,说明氯水中含有氯分子,错误;C、Fe(OH)3胶体的制备方法是将饱和氯化铁溶液逐滴滴加到沸水中至得到红褐色液体,即为Fe(OH)3胶体。向饱和FeCl3溶液中滴加过量氨水,生成Fe(OH)3沉淀,错误;D、将钝化后的铝条放入CuSO4溶液中无现象,是因为氧化铝不与硫酸铜反应,不是说明铝的金属性弱于铜,错误。
考点:考查金属的腐蚀、胶体、氯水的氧化性和金属活动性顺序。

(10分)工业上利用电解污泥(主要含有Fe2O3、CuO、Cr2O3及部分难溶杂质)回收铜和铬等金属,回收流程如下:
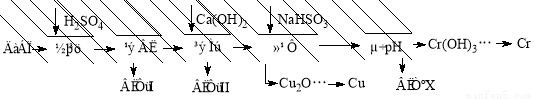
已知部分物质沉淀的pH及CaSO4的溶解度曲线如下:
Fe3+ | Cu2+ | Cr3+ | |
开始沉淀pH | 2.1 | 4.7 | 4.3 |
完全沉淀pH | 3.2 | 6.7 | a |

(1)在浸出过程中除了生成Fe2(SO4)3、Cr2(SO4)3外,主要还有 。
(2)在除铁操作中,需要除去Fe3+和CaSO4,请完成相关操作:①加入石灰乳调节pH范围为: ~ ;②将浊液加热到80℃, 。
(3)写出还原步骤中加入NaHSO3生成Cu2O固体的离子反应方程式 ,此步骤中加入NaHSO3得到Cu2O的产率为95%,若NaHSO3过量,除了浪费试剂外,还会出现的问题是 。



 Fe(SCN)2+(aq) 已知某一条件下,反应达到平衡时,Fe(SCN)2+的物质的量浓度与温度的关系如图所示,下列说法正确的是
Fe(SCN)2+(aq) 已知某一条件下,反应达到平衡时,Fe(SCN)2+的物质的量浓度与温度的关系如图所示,下列说法正确的是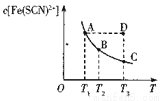
 >
>

 ,室温下实验室用0.01 mol·L-1的氢氧化钠溶液滴定20 mL相同浓度的醋酸溶液,滴定曲线如图所示。下列有关叙述正确的是
,室温下实验室用0.01 mol·L-1的氢氧化钠溶液滴定20 mL相同浓度的醋酸溶液,滴定曲线如图所示。下列有关叙述正确的是