题目内容
磷单质及其化合物的、有广泛应用.
用磷灰石[主要成分]在高温下制备黄磷(P4)的热化学方程式为:
4Ca5(PO4)3F(s)+21SiO2(s)+30C(s)=3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g);△H
①上述反应中,副产物矿渣可用来 .
②已知相同条件下:
4Ca5(PO4)3F(s)+3SiO2(s)=6Ca3(PO4)2(s)+2CaSio3(s)+SiF4(g);△H1
2Ca3(PO4)2(s)+10C(s)=P4(g)+6CaO(s)+10CO(g);△H2
SiO2(s)+CaO(s)=CaSiO3(s);△H3
用△H1、△H2和△H3表示△H,△H= .
用磷灰石[主要成分]在高温下制备黄磷(P4)的热化学方程式为:
4Ca5(PO4)3F(s)+21SiO2(s)+30C(s)=3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g);△H
①上述反应中,副产物矿渣可用来
②已知相同条件下:
4Ca5(PO4)3F(s)+3SiO2(s)=6Ca3(PO4)2(s)+2CaSio3(s)+SiF4(g);△H1
2Ca3(PO4)2(s)+10C(s)=P4(g)+6CaO(s)+10CO(g);△H2
SiO2(s)+CaO(s)=CaSiO3(s);△H3
用△H1、△H2和△H3表示△H,△H=
考点:用盖斯定律进行有关反应热的计算
专题:
分析:①根据硅酸钙可用于制水泥;
②根据已知热化学方程式,利用盖斯定律△H=△H1+3△H2+18△H3进行解答;
②根据已知热化学方程式,利用盖斯定律△H=△H1+3△H2+18△H3进行解答;
解答:
解:①硅酸钙可用于制造水泥,故答案为:水泥;
②热化学方程式4Ca5(PO4)3F(s)+2lSiO2(s)+30C(s)=3P4(g)+20CaSiO3(s)+30CO(g)+SiF4可以将下列三个反应相加得到:4Ca5(PO4)3F(s)+3SiO2(s)=6Ca3(PO4)2(s)+2CaSiO3(s)+SiF4(g)△H1;6Ca3(PO4)2(s)+30C(s)=3P4(g)+18CaO(s)+30CO(g)3△H2;18SiO2(s)+18CaO(s)=18CaSiO3(s)18△H3;根据盖斯定律可得△H=△H1+3△H2+18△H3,
故答案为:△H1+3△H2+18△H3;
②热化学方程式4Ca5(PO4)3F(s)+2lSiO2(s)+30C(s)=3P4(g)+20CaSiO3(s)+30CO(g)+SiF4可以将下列三个反应相加得到:4Ca5(PO4)3F(s)+3SiO2(s)=6Ca3(PO4)2(s)+2CaSiO3(s)+SiF4(g)△H1;6Ca3(PO4)2(s)+30C(s)=3P4(g)+18CaO(s)+30CO(g)3△H2;18SiO2(s)+18CaO(s)=18CaSiO3(s)18△H3;根据盖斯定律可得△H=△H1+3△H2+18△H3,
故答案为:△H1+3△H2+18△H3;
点评:本题考查了热化学方程式含义及反应热的计算,难度不大,掌握盖斯定律是关键.

练习册系列答案
相关题目
下列有关化学用语错误的是( )
A、乙醇分子球棍模型: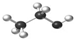 | ||
B、8个中子的碳原子的核素符号:
| ||
C、-OH的电子式: | ||
D、CH4Si的结构式: |
下列物质分子的电子式正确的是( )
A、CH3Cl  |
B、羟基 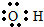 |
C、CO2  |
D、C2H4 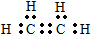 |
假设SiO2原子晶体中的Si原子被Al原子取代,不足的价数用K原子补充.当有25%的Si原子取代时,可形成正长石,则正长石的化学组成为( )
| A、KAlSiO4 |
| B、KAlSi2O4 |
| C、KAlSi3O8 |
| D、KAlSi4O10 |
下列单体能在一定条件下加聚反应生成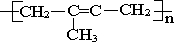 的是( )
的是( )
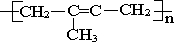 的是( )
的是( )| A、丙烯 |
| B、2-甲基-1,3-丁二烯 |
| C、乙烯和丙烯 |
| D、2-甲基-2-丁烯 |
分子式为C8H10O的有机物有多种同分异构体,其中属于醇且苯环上有2个取代基的同分异构体有( )种.
| A、3种 | B、4种 | C、5种 | D、6种 |
 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液,在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液,在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: