题目内容
8.对于物质的量相同的硫酸(H2SO4)和磷酸(H3PO4),下列说法中不正确的是( )| A. | 分子数相同 | B. | 氧原子个数相等 | C. | 氢原子个数相等 | D. | 质量相等 |
分析 A.分子数目之比等于其物质的量之比;
B.一个硫酸分子中4个氧原子,一个磷酸分子中有4个氧原子;
C.一个硫酸分子中2个氢原子,一个磷酸分子中有3个氢原子;
D.根据m=nM判断.
解答 解:A.根据N=nNA可知,二者物质的量相等,含有分子数目相等,故A正确;
B.一个硫酸分子中4个氧原子,一个磷酸分子中有4个氧原子,二者物质的量相同,含有氧原子个数相同,故B正确;
C.一个硫酸分子中2个氢原子,一个磷酸分子中有3个氢原子,二者物质的量相同,含有H原子数目之比为2:3,含有氢原子数目不相等,故C错误;
D.H2SO4、H3PO4的摩尔质量均为98g/mol,二者物质的量相等,根据m=nM可知二者质量相等,故D正确,
故选C.
点评 本题考查物质的量有关计算,侧重对微粒数目的计算考查,比较基础,注意对化学式意义的理解.

练习册系列答案
相关题目
18.下列说法正确的是( )
| A. | 甲烷的燃烧热为 890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol | |
| B. | 500℃、30 MPa 下,将 0.5 mol N2 和 1.5 mol H2 置于密闭的容器中充分反应生成 NH3(g),放热 19.3 kJ,其热化学方程式为 N2(g)+3H2(g)?2NH2(g)△H=-38.6 kJ•mol | |
| C. | 一定条件下,反应 N2(g)+3H2(g)?2NH3(g)△H=-38.6 kJ•mol降低温度将向正反应方向移动 | |
| D. | 已知 2C(s)+2O2(g)═2CO2(g)△H12C(s)+O2(g)═2CO(g)△H2,则△H1>△H2 |
16. 如表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
如表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
 如表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
如表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )| A. | X、Y、Z的阴离子电子层结构均与R原子的相同 | |
| B. | 常压下,Y单质的沸点比Z单质的沸点高 | |
| C. | W的氢化物的稳定性比X的氢化物的稳定性强 | |
| D. | 最高价氧化物的水化物酸性W比Y强 |
3.可逆反应N2O4?2NO2△H>0在密闭容器中反应,达到平衡状态,要使混合气体颜色加深,可采取的方法是( )
①选用合适的催化剂; ②缩小体积; ③升高温度; ④增大N2O4的浓度.
①选用合适的催化剂; ②缩小体积; ③升高温度; ④增大N2O4的浓度.
| A. | ③④ | B. | ①②③ | C. | ②③④ | D. | ①④ |
20.下列实验现象描述错误的是( )
| A. | 硫在空气中燃烧,产生蓝紫色火焰 | |
| B. | 将二氧化碳通入水中,无明显现象 | |
| C. | 红亮的铜丝在酒精灯火焰上灼烧,铜丝表面变黑 | |
| D. | 一氧化碳通过灼热的氧化铁,红色固体变黑 |
17.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 14g 乙烯和丁烯的混合物中含有3NA对共用电子对 | |
| B. | 1mol苯中含有3NA个碳碳双键 | |
| C. | 乙烷与Cl2在光照下反应,每有NA个氢原子被氯替代,需消耗标准状况下Cl2 11.2L | |
| D. | 标准状况下,22.4L己烷中的碳原子数为6NA |
10.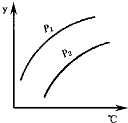 如图表示不同温度和压强下,对可逆反应2L(气)?2M(气)+N(气)△H>0平衡状态的影响(p1<p2),图中y轴表示的意义是( )
如图表示不同温度和压强下,对可逆反应2L(气)?2M(气)+N(气)△H>0平衡状态的影响(p1<p2),图中y轴表示的意义是( )
 如图表示不同温度和压强下,对可逆反应2L(气)?2M(气)+N(气)△H>0平衡状态的影响(p1<p2),图中y轴表示的意义是( )
如图表示不同温度和压强下,对可逆反应2L(气)?2M(气)+N(气)△H>0平衡状态的影响(p1<p2),图中y轴表示的意义是( )| A. | 一定条件下L的转化率 | B. | 气体混合物的平均摩尔质量 | ||
| C. | 气体混合物中L的体积分数 | D. | 气体L的物质的量 |