题目内容
2.下列叙述正确的是( )| A. | 常温常压下,1.5 mol N2的体积约为33.6 L | |
| B. | NaOH的摩尔质量是40 g | |
| C. | 150mL 1 mol/LNaCl溶液与100mL 1 mol/LAlCl3溶液中的n(Cl-)相等 | |
| D. | 同温同压下,相同体积的C12和SO2气体所含的分子数一定相同 |
分析 A、标准状况下,1.5 mol N2的体积约为33.6 L;
B、摩尔质量g/mol;
C、根据n=cV进行计算求解;
D、同温同压下,气体摩尔体积相等,根据V=nVm知,体积之比等于物质的量之比.
解答 解:A、标准状况下,1.5 mol N2的体积约为33.6 L,而不是常温常压下,故A错误;
B、摩尔质量g/mol,所以NaOH的摩尔质量是40g/mol,故B错误;
C、150mL 1 mol/LNaCl溶液中的n(Cl-)=0.15mol,100mL 1 mol/LAlCl3溶液中的n(Cl-)=0.1×3=0.3mol,所以两者的量不等,故C错误;
D、同温同压下,气体摩尔体积相等,根据V=nVm知,体积之比等于物质的量之比,所以物质的量为1:1,则同温同压下,相同体积的C12和SO2气体所含的分子数一定相同,故D正确;
故选D.
点评 本题考查阿伏伽德罗定律及其推论,明确物质的量公式中各个物理量的关系是解本题关键,熟练掌握物质的量有关公式,题目难度不大.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
12.下列性质中不是所有金属共有的是( )
| A. | 不透明 | B. | 易与氧气反应 | C. | 易导热 | D. | 易导电 |
17.下列关于硅酸的说法正确的是( )
| A. | 硅酸可以通过SiO2和水化合反应直接制得 | |
| B. | 可用反应Na2SiO3+2HCl═2NaCl+H2SiO3↓制取硅酸 | |
| C. | 因为硅酸难溶于水,所以它不能与NaOH溶液反应 | |
| D. | 干燥剂“硅胶”的主要成分是硅酸钠 |
11.实脸室取等物质的量的KClO3分别发生下述反应:
反应一:有催化剂存在时,受热分解得到氧气;
反应二:不使用催化剂,加热至743K左右,得到KClO4和KCl.
下列关于①和②的说法正确的是( )
反应一:有催化剂存在时,受热分解得到氧气;
反应二:不使用催化剂,加热至743K左右,得到KClO4和KCl.
下列关于①和②的说法正确的是( )
| A. | 两个反应中都只有一种元素化合价发生改变 | |
| B. | 两个过程生成KCl的物质的量相同 | |
| C. | 发生氧化反应的元素相同 | |
| D. | 发生还原反应的元素相同 |
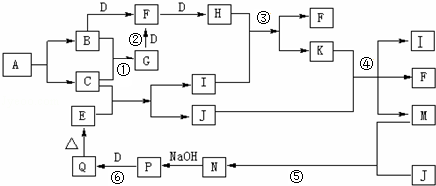
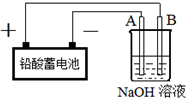 Cu2O是一种半导体材料,实验室用铅酸蓄电池电解一定浓度的NaOH溶液制备Cu2O,方程式为2Cu+H2O$\frac{\underline{\;电解\;}}{\;}$Cu2O+H2↑装置如图所示,回答下列问题
Cu2O是一种半导体材料,实验室用铅酸蓄电池电解一定浓度的NaOH溶液制备Cu2O,方程式为2Cu+H2O$\frac{\underline{\;电解\;}}{\;}$Cu2O+H2↑装置如图所示,回答下列问题 某同学设计了如图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请根据下列实验回答问题:
某同学设计了如图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请根据下列实验回答问题: