题目内容
11.根据下列叙述,写出微粒符号和微粒结构示意图.(1)原子核外有2个电子层,核外有10个电子的原子:Ne、
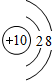 .
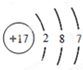
.(2)原子核外有3个电子层,最外层有7个电子的原子:Cl、
 .
.(3)最外层电子数是次外层电子数4倍的二价阴离子:O2-、
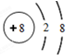
(4)电子总数为18的一价简单阳离子:K+、
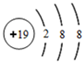 .
.
分析 (1)核外有10个电子的原子为Ne,根据其质子数和电子数画出原子结构示意图;
(2)原子核外有3个电子层,最外层有7个电子,为Cl,根据其质子数和电子数画出原子结构示意图;
(3)最外层电子数是次外层电子数4倍的二价阴离子为O2-;根据其质子数和电子数画出原子结构示意图
(4)电子总数为18的一价简单阳离子为K+,根据其质子数和电子数画出原子结构示意图.
解答 解:(1)核外有10个电子的原子为Ne,其质子数为10和电子数为10,原子结构示意图: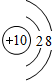 ,故答案为:Ne;
,故答案为:Ne;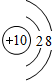 ;
;
(2)原子核外有3个电子层,最外层有7个电子,为Cl,其质子数为17,电子数为17,则原子结构示意图: ,故答案为:Cl;
,故答案为:Cl; ;
;
(3)最外层电子数是次外层电子数4倍的二价阴离子为O2-,其质子数为8,核外电子数为10,则原子结构示意图: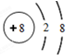 ,故答案为:O2-;
,故答案为:O2-;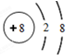 ;
;
(4)电子总数为18的一价简单阳离子为K+,其质子数为19,核外电子数为18,则离子结构示意图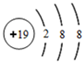 ,故答案为:K+;
,故答案为:K+;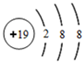 .
.
点评 本题考查了元素的推断和原子结构示意图,题目比较简单,明确原子或离子的质子数和电子数的关系即可解答.

练习册系列答案
相关题目
1.已知CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-Q1 kJ•mol-12H2(g)+O2(g)═2H2O(g)△H=-Q2 kJ•mol-12H2(g)+O2(g)═2H2O(l)△H=-Q3 kJ•mol-1常温下,取体积比为4:1的甲烷和氢气的混合气体11.2L(标准状况)经完全燃烧后恢复到常温,则放出的热量为( )
| A. | (0.4 Q1+0.05 Q3) kJ | B. | (0.4 Q1+0.05 Q2) kJ | ||
| C. | (0.4 Q1+0.1 Q3) kJ | D. | (0.4Q1+0.2 Q1) kJ |
2.北京2008年奥运会在开幕式之前举行的隆重的火炬接力仪式.火炬的可燃物为丁烷(C4H10).下列关于丁烷的说法中,不正确的是( )
| A. | 丁烷中碳、氢原子的个数比为4:10 | |
| B. | 丁烷中碳、氢两种元素的质量比是4:10 | |
| C. | 丁烷由碳、氢两种元素组成 | |
| D. | 一个丁烷分子由4个碳原子和10个氢原子构成 |
16.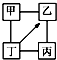 图中“-”表示相连的物质间在一定条件下可以反应,“-→”表示丁在一定条件下可以转化为乙.下面四组选项中,符合图示要求的是( )
图中“-”表示相连的物质间在一定条件下可以反应,“-→”表示丁在一定条件下可以转化为乙.下面四组选项中,符合图示要求的是( )
 图中“-”表示相连的物质间在一定条件下可以反应,“-→”表示丁在一定条件下可以转化为乙.下面四组选项中,符合图示要求的是( )
图中“-”表示相连的物质间在一定条件下可以反应,“-→”表示丁在一定条件下可以转化为乙.下面四组选项中,符合图示要求的是( )| 甲 | 乙 | 丙 | 丁 | |
| A | H2SO4 | Na2SO4 | NaOH | NaCl |
| B | KCl | K2CO3 | KOH | HCl |
| C | O2 | CO | CuO | C |
| D | Fe | CuCl2 | Zn | HCl |
| A. | A | B. | B | C. | C | D. | D |
3.荧光素是发光物质的基质,5-羧基荧光素与5-羧基荧光素二乙酸酯在碱性条件下有强烈的绿色荧光,它们广泛应用于荧光分析等.下列说法正确的是( )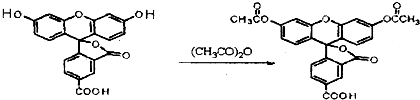
5-羧基荧光素(5-FAM) 5-羧基荧光素二乙酸酯(5-CFDA)
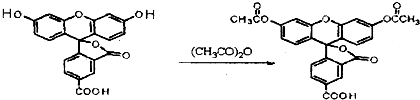
5-羧基荧光素(5-FAM) 5-羧基荧光素二乙酸酯(5-CFDA)
| A. | 5-FAM转变为5-CFDA属于取代反应 | |
| B. | 实验室鉴别5-FAM与5-CFDA可用碳酸氢钠溶液 | |
| C. | 5-FAM的分子式为:C21H3O7 | |
| D. | 5-FAM和5-CFDA分子中的所有原子均共面 |
1.下列说法不正确的是( )
| A. | 在稀硫酸中加入铜粉,铜粉不溶解,再加入Cu(NO3)2固体,铜粉仍不溶解 | |
| B. | 某气体能使湿润的红色石蕊试纸变蓝,该气体的水溶液一定显碱性 | |
| C. | 铜与稀硝酸反应的离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O | |
| D. | HNO3→NO→NO2,以上各步变化均能通过一步实现 |
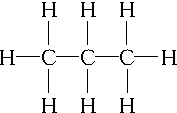 ,C3H6的同分异构体为CH2═CH-CH3、
,C3H6的同分异构体为CH2═CH-CH3、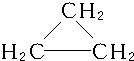 .
.