题目内容
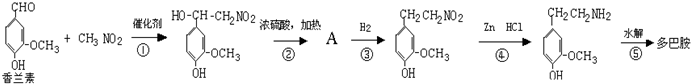
 在下面的装置中,A是Cl2发生装置,C、D为气体净化装置,C中装有饱和NaCl溶液,D中装有浓H2SO4;E硬质玻璃管中装有细铁丝网;F为干燥的空广口瓶;烧杯G为尾气吸收装置.
在下面的装置中,A是Cl2发生装置,C、D为气体净化装置,C中装有饱和NaCl溶液,D中装有浓H2SO4;E硬质玻璃管中装有细铁丝网;F为干燥的空广口瓶;烧杯G为尾气吸收装置.试回答:
(1)C、D两个装置的作用是:C
(2)E中的现象为
(3)写出在A、E、G中发生反应的化学方程式为:
A:
E:
G:
考点:性质实验方案的设计
专题:实验设计题
分析:实验室制取Cl2通常利用下面的反应原理:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,在如图的装置中,A是Cl2发生装置,B中是浓盐酸,A中是MnO2,C、D为气体的净化装置,C中装有饱和食盐水除去氯气中的氯化氢,D中装有浓H2SO4,是吸收氯气中的水蒸气,E是硬质玻璃管中装有细铁丝网,氯气通过会发生反应生成氯化铁,F为干燥的广口瓶是用来收集氯气的集气瓶,烧杯G为尾气吸收装置,氢氧化钠溶液吸收防止氯气污染空气,以此解答该题.
| ||
解答:
解:实验室制取Cl2通常利用下面的反应原理:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,在如图的装置中,A是Cl2发生装置,B中是浓盐酸,A中是MnO2,C、D为气体的净化装置,C中装有饱和食盐水除去氯气中的氯化氢,D中装有浓H2SO4,是吸收氯气中的水蒸气,E是硬质玻璃管中装有细铁丝网,氯气通过会发生反应生成氯化铁,F为干燥的广口瓶是用来收集氯气的集气瓶,烧杯G为尾气吸收装置,氢氧化钠溶液吸收防止氯气污染空气,
(1)实验制备氯气中含杂质气体氯化氢和水蒸气,氯化氢易溶于饱和氯化钠溶,而饱和氯化钠溶液中含有大量的氯离子,抑制氯气的溶解,通过饱和食盐水可以除去氯气中的氯化氢,浓硫酸具有吸水性,通过浓硫酸可以除去氯气中的水蒸气;
故答案为:除去Cl2中的HCl杂质;干燥Cl2;
(2)铁丝在氯气中燃烧,放出大量的棕红色的烟,生成氯化铁固体,故答案为:充满棕黄色的烟;FeCl3;
(3)二氧化锰与浓盐酸反应生成氯化锰、氯气和水,化学方程式为:MnO2+4HCl
MnCl2+Cl2↑+2H2O;
氯气与铁反应生成氯化铁,化学方程式为:3Cl2+2Fe
2FeCl3;
氯气与氢氧化钠反应生成氯化钠和次氯酸钠、水,离子方程式为:Cl2+2NaOH═NaCl+NClO+H2O;
故答案为:MnO2+4HCl
MnCl2+Cl2↑+2H2O;3Cl2+2Fe
2FeCl3;Cl2+2NaOH═NaCl+NClO+H2O.
| ||
(1)实验制备氯气中含杂质气体氯化氢和水蒸气,氯化氢易溶于饱和氯化钠溶,而饱和氯化钠溶液中含有大量的氯离子,抑制氯气的溶解,通过饱和食盐水可以除去氯气中的氯化氢,浓硫酸具有吸水性,通过浓硫酸可以除去氯气中的水蒸气;
故答案为:除去Cl2中的HCl杂质;干燥Cl2;
(2)铁丝在氯气中燃烧,放出大量的棕红色的烟,生成氯化铁固体,故答案为:充满棕黄色的烟;FeCl3;
(3)二氧化锰与浓盐酸反应生成氯化锰、氯气和水,化学方程式为:MnO2+4HCl
| ||
氯气与铁反应生成氯化铁,化学方程式为:3Cl2+2Fe
| ||
氯气与氢氧化钠反应生成氯化钠和次氯酸钠、水,离子方程式为:Cl2+2NaOH═NaCl+NClO+H2O;
故答案为:MnO2+4HCl
| ||
| ||
点评:本题考查了氯气的制备和性质的检验,为高频考点,侧重学生的分析、实验能力的考查,明确氯气制备的原理和氯气的性质是解题关键,注意二氧化锰只与浓盐酸反应,题目难度不大.

练习册系列答案
相关题目
往CuO和Fe粉的混合物中,加入一定量的稀硫酸,并微热,当反应停止后,滤出不溶物,并向滤液中插入一枚光亮的铁钉,片刻后,取出铁钉,发现铁钉无任何变化.根据上述现象,确定下面结论正确的是( )
| A、滤出的不溶物一定是铜 |
| B、滤出的不溶物一定含铜,但不一定含铁 |
| C、滤出的不溶物一定是铁 |
| D、滤液中一定含有Fe2+和Cu2+ |
最新研究表明生命起源于火山爆发,是因为火山爆发产生的气体中含有1%的羰基硫(OCS),已知羰基硫中所有原子均满足8电子稳定结构.下列有关羰基硫的说法正确的是( )
| A、属于非极性分子 |
| B、沸点低于CO2 |
C、电子式为  |
| D、三个原子位于同一直线上 |
下列碳族元素(ⅣA)的名称与符号对应不正确的是( )
| A、碳(C) | B、硅(Si) |
| C、锗(Sn) | D、铅(Pb) |
下列反应中,以苯作原料,通过加成反应制得的是( )
| A、溴苯 | B、硝基苯 |
| C、苯磺酸 | D、环己烷 |
下列叙述错误的是( )
| A、用金属钠可区分乙醇和乙烷 |
| B、用高锰酸钾酸性溶液可区分己烷和己烯 |
| C、用水可区分苯和溴苯 |
| D、用饱和食盐水可区分乙醇和乙酸 |
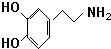
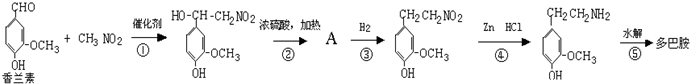 (3)多巴胺可由香兰素与硝基甲烷缩合,再经锌-盐酸还原水解而得.合成过程表示如下:
(3)多巴胺可由香兰素与硝基甲烷缩合,再经锌-盐酸还原水解而得.合成过程表示如下: