题目内容
A、B、C、D四种短周期元素,它们的核电荷数依次增大;A元素原子核外只有一个电子;C元素的焰色反应呈黄色;B元素原子L层电子数是K层电子数的3倍;D原子核中的质子数比C多6个.
回答:
(1)A是 ,B是 .
(2)C元素最高价氧化物对应水化物的化学式为 .
(3)C和D形成的化合物的化学键类型为 .(填“离子键”或“共价键”)
(4)D元素在周期表中的位置是第 周期第 族.
回答:
(1)A是
(2)C元素最高价氧化物对应水化物的化学式为
(3)C和D形成的化合物的化学键类型为
(4)D元素在周期表中的位置是第
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:A、B、C、D四种短周期元素,它们的核电荷数依次增大;A元素原子核外只有一个电子,则A为氢元素;C元素的焰色反应呈黄色,则C为Na;B元素原子L层电子数是K层电子数的3倍,则L层电子数为6,故B为氧元素;D原子核中的质子数比C多6个,则D原子质子数=11+6=17,故D为Cl,据此解答.
解答:
解:A、B、C、D四种短周期元素,它们的核电荷数依次增大;A元素原子核外只有一个电子,则A为氢元素;C元素的焰色反应呈黄色,则C为Na;B元素原子L层电子数是K层电子数的3倍,则L层电子数为6,故B为氧元素;D原子核中的质子数比C多6个,则D原子质子数=11+6=17,故D为Cl,
(1)由上述分析可知,A是H,B是O,故答案为:H;O;
(2)C为Na元素,最高价氧化物对应水化物的化学式为NaOH,故答案为:NaOH;
(3)C和D形成的化合物为NaCl,属于离子化合物,含有离子键,故答案为:离子键;
(4)D为Cl元素,原子核外有3个电子层、最外层电子数为7,在周期表中的位置是第三周期第ⅦA族,故答案为:三;ⅦA.
(1)由上述分析可知,A是H,B是O,故答案为:H;O;
(2)C为Na元素,最高价氧化物对应水化物的化学式为NaOH,故答案为:NaOH;
(3)C和D形成的化合物为NaCl,属于离子化合物,含有离子键,故答案为:离子键;
(4)D为Cl元素,原子核外有3个电子层、最外层电子数为7,在周期表中的位置是第三周期第ⅦA族,故答案为:三;ⅦA.
点评:本题考查结构性质位置关系应用,推断元素是解题关键,侧重对基础知识的巩固,比较基础.

练习册系列答案
相关题目
在2升的密闭容器中,反应物的物质的量为3mol,经过20s后,它的物质的量变成了1mol,在这20s内它的反应速率为( )
| A、0.1 mol/(L?S) |
| B、0.05mol/( L?min) |
| C、0.05mol/(L?s) |
| D、0.8mol/(L?S) |
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
| A、氢氧燃料电池在碱性介质中的负极反应式:O2+2H2O+4e-=4OH- |
| B、钢铁发生电化学腐蚀的负极反应式:Fe一3e-=Fe3+ |
| C、粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu一2e-=Cu2+ |
| D、Pt电极电解饱和食盐水时,阳极的电极反应式为:2Cl-一2e-=Cl2↑ |
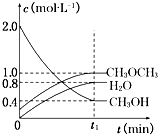 (1)一定条件下,NO与NO2存在下列反应:NO(g)+NO2(g)?N2O3(g),其平衡常数表达式为K=
(1)一定条件下,NO与NO2存在下列反应:NO(g)+NO2(g)?N2O3(g),其平衡常数表达式为K= 新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入 CH4和 O2,电解质为 KOH 溶液.某研究小组将甲烷燃料电 池作为电源进行氯化镁溶液龟解实验,电解装置如图所示.
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入 CH4和 O2,电解质为 KOH 溶液.某研究小组将甲烷燃料电 池作为电源进行氯化镁溶液龟解实验,电解装置如图所示.
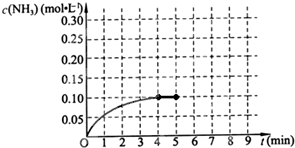 在一容积为2L的密闭容器中,加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g);△H<0,反应中NH3的物质的量浓度的变化情况如图所示,请回答下列问题:
在一容积为2L的密闭容器中,加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g);△H<0,反应中NH3的物质的量浓度的变化情况如图所示,请回答下列问题: