题目内容
5.金属镍及其化合物在合金材料以及催化剂等方面应用广泛,Ni的基态原子有7种能量不同的电子;很多不饱和有机物在Ni催化下可以H2发生加成反应,如①CH2═CH2、②HC≡CH、③ 、④HCHO等,其中碳原子不是采取sp2杂化的分子有②(填物质编号),HCHO分子的立体构型为平面三角形.
、④HCHO等,其中碳原子不是采取sp2杂化的分子有②(填物质编号),HCHO分子的立体构型为平面三角形.
分析 Ni的基态原子核外电子排布式为1s22s22p63s23p63d84s2,同一能级轨道上的电子能量相同;CH2=CH2、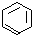 、HCHO中碳原子均形成3个σ键、没有孤对电子,杂化轨道数目为3,而HC≡CH中碳原子均形成2个σ键、没有孤对电子,杂化轨道数目为2.
、HCHO中碳原子均形成3个σ键、没有孤对电子,杂化轨道数目为3,而HC≡CH中碳原子均形成2个σ键、没有孤对电子,杂化轨道数目为2.
解答 解:Ni的基态原子核外电子排布式为1s22s22p63s23p63d84s2,同一能级轨道上的电子能量相同,则原子有7种能量不同的电子;CH2=CH2、 、HCHO中碳原子均形成3个σ键、没有孤对电子,杂化轨道数目为3,碳原子采取sp2杂化,HCHO的空间构型为平面三角形,而HC≡CH中碳原子均形成2个σ键、没有孤对电子,杂化轨道数目为2,碳原子采取sp杂化,
、HCHO中碳原子均形成3个σ键、没有孤对电子,杂化轨道数目为3,碳原子采取sp2杂化,HCHO的空间构型为平面三角形,而HC≡CH中碳原子均形成2个σ键、没有孤对电子,杂化轨道数目为2,碳原子采取sp杂化,
故答案为:7;②;平面三角形.
点评 本题考查核外电子排布规律、杂化方式与空间构型判断,注意对基本概念的理解,题目难度适中.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
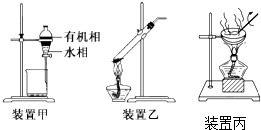
8.下列实验操作正确的是( )

| A. | 用玻璃棒蘸取CH3COOH溶液点在水湿润的pH试纸上,测定该溶液的pH | |
| B. | 用装置甲分液,放出水相后再从分液漏斗上口放出有机相 | |
| C. | 用装置乙加热分解NaHCO3固体 | |
| D. | 用装置丙加热硫酸铜溶液获得CuSO45H2O |
10.设NA为阿伏加德罗常数的数值.下列叙述正确的是( )
| A. | 完全氧化56gFe需要消耗氯气33.6 L | |
| B. | 某浓度氢氧化钠溶液恰好溶解5.4g的铝,则被还原的水的分子数为0.6NA | |
| C. | 向100mL 1mol/L的NaHSO3溶液中加入足量的硫酸铁,则反应后氢离子增加0.4mol | |
| D. | 利用铝热反应将磁铁矿还原得到16.8g铁单质,反应中Fe得到了0.9 NA电子 |
17.下列元素中,最高正化合价数值最大的是( )
| A. | Si | B. | N | C. | O | D. | Ar |
