题目内容
15.氯化铵常用作焊接.如:在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,其反应为:4CuO+2NH4Cl→3Cu+1CuCl2+N2↑+4H2O
(1)配平此氧化还原反应方程式.
(2)该反应中,被氧化的元素是氮(填元素名称),氧化剂是CuO(填化学式).
分析 CuO+NH4Cl→Cu+CuCl2+N2↑+H2O中,Cu元素的化合价由+2价降低为0,N元素的化合价由-3价升高为0,结合电子、原子守恒解答.
解答 解:(1)CuO+NH4Cl→Cu+CuCl2+N2↑+H2O中,Cu元素的化合价由+2价降低为0,N元素的化合价由-3价升高为0,由电子、原子守恒可知该氧化还原反应为4CuO+2NH4Cl=3Cu+CuCl2+N2↑+4H2O,故答案为:4;2;3;1;4;
(2)该反应中N失去电子可知氮元素被氧化,Cu元素的化合价降低,则氧化剂为CuO,故答案为:氮; CuO.
点评 本题考查氧化还原反应及配平,为高频考点,把握反应中元素的化合价变化、电子和原子守恒为解答的关键,注意守恒法的应用,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.锂水电池以金属锂和钢板为电极材料,LiOH为电解质,使用时加入水即可放电.关于该电池的说法正确的是( )
| A. | 钢板是正极,正极上发生还原反应 | |
| B. | 放电时电子的流向:正极→导线→负极 | |
| C. | 放电时OH-向正极移动 | |
| D. | 放电时总反应为:4Li+2H2O+O2=4LiOH |
10.含11.2g KOH的稀溶液与1L 0.1mol/L的H2SO4溶液反应放出11.46kJ的热量,下列能正确表示中和热的热化学方程式是( )
| A. | 2KOH(aq)+H2SO4(aq)=K2SO4(aq)+2H2O (l);△H=-114.6kJ/mol | |
| B. | KOH(s)+$\frac{1}{2}$H2SO4(aq)=$\frac{1}{2}$K2SO4(aq)+H2O (l);△H=-57.3 kJ/mol | |
| C. | 2KOH(s)+H2SO4(aq)=K2SO4(aq)+2H2O (l);△H=-114.6 kJ/mol | |
| D. | KOH(aq)+$\frac{1}{2}$ H2SO4(aq)=$\frac{1}{2}$K2SO4(aq)+H2O (l);△H=-57.3kJ/mol |
20.向一定量的Fe、FeO、Fe2O3、Fe3O4的混合物中加入150mL 4mol•L-1的稀硝酸恰好使混合物完全溶解,放出2.24L NO(标准状况),往所得溶液中加入KSCN溶液,无血红色出现.若用足量的H2在加热条件下还原相同质量的混合物,所得到的铁的物质的量为( )
| A. | 0.21 mol | B. | 0.25 mol | C. | 0.3 mol | D. | 0.35 mol |
7.下列说法错误的是( )
| A. | 需要加热方能发生的反应一定是吸热反应 | |
| B. | 放热的反应在常温下一定很容易发生 | |
| C. | 反应是放热还是吸热必须看反应物和生成物所具有总能量的相对大小 | |
| D. | 吸热反应在一定的条件下也能发生 |
5.下列关于元素及其化合物的说法不正确的是( )
| A. | 过氧化钠放置在空气中,最终转变为白色粉末Na2CO3 | |
| B. | Ca(ClO)2溶液通入CO2,溶液变浑浊;再加入品红溶液,红色褪去 | |
| C. | 打磨过的铝箔和未打磨的铝箔分别在空气中灼烧,两种铝箔均熔化但不滴落,说明氧化铝熔点比铝高 | |
| D. | 在一定条件下,金属Na、Mg、Fe与水反应都生成H2和对应的碱 |
 、④HCHO等,其中碳原子不是采取sp2杂化的分子有②(填物质编号),HCHO分子的立体构型为平面三角形.
、④HCHO等,其中碳原子不是采取sp2杂化的分子有②(填物质编号),HCHO分子的立体构型为平面三角形.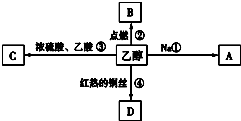 乙醇是生活中常见的有机物,能进行如图所示的多种反应,A、B、C、D都是含碳的化合物.
乙醇是生活中常见的有机物,能进行如图所示的多种反应,A、B、C、D都是含碳的化合物.