题目内容
14.在一定条件下,对于密闭容器中进行的可逆反应:N2(g)+3H2(g) $?_{△}^{催化剂}$2NH3(g)在2分钟内NH3的反应速率为0.6mol/(L•min),则H2的反应速率为( )| A. | 0.3 mol/L•min | B. | 0.6 mol/(L•min) | C. | 0.9 mol/(L•min) | D. | 1.2 mol/L•min |
分析 结合反应速率之比等于化学计量数之比计算.
解答 解:2分钟内NH3的反应速率为0.6mol/(L•min),由反应速率之比等于化学计量数之比可知,H2的反应速率为0.6mol/(L•min)×$\frac{3}{2}$=0.9 mol/(L•min),
故选C.
点评 本题考查化学反应速率的计算,为高频考点,把握反应速率与化学计量数的关系为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
4.锂硅合金-二硫化亚铁电池是一种高能电池,总反应式为:4Li+FeS2═Fe+2Li2S.用该电池为电源电解200mL浓度均为0.1mol/L 的NaCl和CuSO4的混合溶液,当电池消耗1.2g FeS2时,下列有关叙述不正确的是( )
| A. | 该电池不能用水溶液作为电解质 | |
| B. | 阳极产生的气体为Cl2和O2 | |
| C. | 电解后该溶液的pH=2 | |
| D. | 电源正极的电极反应式为:FeS2+4e-═Fe+2S2- |
5.如图所示的原电池中,锌电极为( )
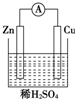

| A. | 负极 | B. | 正极 | ||
| C. | 发生还原反应的一极 | D. | 发生氧化反应的一极 |
2.用NA表示阿伏加德罗常数的值,下列判断正确的是( )
| A. | 46 g 14CO2含氧原子数为2 NA | |
| B. | 1 mol Fe与足量的浓盐酸完全反应时转移电子数为3 NA | |
| C. | 标准状况下,22.4 L CCl4含有的分子数目为NA | |
| D. | 1 mol•L-1 CuCl2溶液中含Cl-数目为2 NA |
9.下列仪器可用酒精灯直接加热的是( )
| A. | 量筒 | B. | 分液漏斗 | C. | 试管 | D. | 容量瓶 |
19.如表是元素周期表的一部分,针对表中的①~⑩元素,回答下列问题:
(1)在这些元素中,非金属性最强的元素符号是F;
(2)⑧元素的氢化物的化学式为SiH4;
(3)金属性最活泼的元素的原子结构示意图为 ;
;
(4)能用来雕刻玻璃的氢化物的化学式是HF;
(5)④、⑨、⑩三种元素的原子半径由大到小的排列顺序为S>Cl>F(用元素符号表示);
(6)写出③元素的气态氢化物和⑨元素的最高价氧化物对应水化物相互反应的化学方程式2NH3+H2SO4=(NH4)2SO4;
(7)在⑤、⑥、⑦三种元素中,最高价氧化物对应的水化物的碱性最强的是NaOH(用化学式表示);
(8)能证明元素⑩比元素⑨的非金属性强的事实是BC(填序号).
A.常温下⑩单质的密度小于⑨单质的密度
B.⑩元素的气态氢化物比⑨元素的气态氢化物更稳定
C.⑩单质与氢气反应的程度比⑨单质与氢气反应的程度更剧烈
D.⑨元素的最高价氧化物对应的水化物酸性强于⑩元素的最高价氧化物对应的水化物.
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 一 | ① | ||||||
| 二 | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)⑧元素的氢化物的化学式为SiH4;
(3)金属性最活泼的元素的原子结构示意图为
 ;
;(4)能用来雕刻玻璃的氢化物的化学式是HF;
(5)④、⑨、⑩三种元素的原子半径由大到小的排列顺序为S>Cl>F(用元素符号表示);
(6)写出③元素的气态氢化物和⑨元素的最高价氧化物对应水化物相互反应的化学方程式2NH3+H2SO4=(NH4)2SO4;
(7)在⑤、⑥、⑦三种元素中,最高价氧化物对应的水化物的碱性最强的是NaOH(用化学式表示);
(8)能证明元素⑩比元素⑨的非金属性强的事实是BC(填序号).
A.常温下⑩单质的密度小于⑨单质的密度
B.⑩元素的气态氢化物比⑨元素的气态氢化物更稳定
C.⑩单质与氢气反应的程度比⑨单质与氢气反应的程度更剧烈
D.⑨元素的最高价氧化物对应的水化物酸性强于⑩元素的最高价氧化物对应的水化物.
4.下列说法不正确的是( )
| A. | ${\;}_{2}^{3}$He的中子数是2 | B. | 白磷、红磷互为同素异形体 | ||
| C. | 18O和16O是互为同位素 | D. | 正丁烷和异丁烷互为同分异构体 |