题目内容
已知空气-锌电池的电极反应为:锌片:2Zn+4OH--4e-=2ZnO+2H2O;碳棒:O2+2H2O+4e-=4OH-,据此判断,锌片是( )
| A、正极,被还原 |
| B、正极,被氧化 |
| C、负极,被还原 |
| D、负极,被氧化 |
考点:原电池和电解池的工作原理
专题:
分析:根据化合价变化判断氧化还原反应,原电池中较活泼的金属做负极,发生氧化反应.
解答:
解:锌片:2Zn+4OH--4e-=2ZnO+2H2O,电极反应中锌的化合价升高,被氧化,原电池中较活泼的金属做负极,发生氧化反应,则锌为原电池的负极,被氧化.
故选:D.
故选:D.
点评:本题考查化学电源知识,题目难度不大,注意原电池的两极上的变化以及原电池原理.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
下列说法正确的是( )
| A、淀粉、油脂、蛋白质都能水解,但水解产物不同 |
| B、乙醇和油脂都能与氢氧化钠溶液反应 |
| C、淀粉、纤维素化学式均为(C6H10O5)n,互为同分异构体 |
| D、乙烯和苯均能与溴水发生加成反应 |
下列物质中含有自由移动的Cl-离子的是( )
| A、KClO3溶液 |
| B、MgCl2溶液 |
| C、液态HCl |
| D、NaCl固体 |
下列说法中正确的是(NA表示阿伏加德罗常数的值)( )
| A、常温下,28gFe与足量的浓硝酸反应,转移的电子数为1.5NA |
| B、标准状况下,含4molHCl的浓盐酸与足量MnO2反应可生成22.4LCl2 |
| C、3.2g铜在硫蒸气中完全燃烧,转移的电子数为0.1NA |
| D、常温常压下,0.1mol氖气含有的电子数为NA |
下列反应中,水作还原剂的是( )
| A、2Na+2H2O=2NaOH+H2↑ |
| B、2Na2O2+2H2O=4NaOH+O2↑ |
| C、3NO2+H2O=2HNO3+NO |
| D、2Cl2+2H2O=4HCl+O2 |
A、B、C三种短周期元素在元素周期表中的相对位置如图所示,已知A、C可分别与B形成化合物X和Y,A与B的质子数之和为C的质子数,以下说法中不正确的是( )
| A | B |
| C |
| A、B与C均存在同素异形体 |
| B、X的种类比Y的多 |
| C、C的最高价氧化物对应水化物能与A的氢化物形成三种盐 |
| D、沸点:A的氢化物低于C的氢化物 |
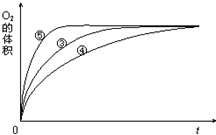 某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.
某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.