题目内容
10.25℃时,如果取0.1mol•L-1HA溶液与0.1mol•L-1NaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8,试回答以下问题:(1)混合溶液的pH=8的原因是A-+H2O?HA+OH-(用离子方程式表示);
(2)混合溶液中由水电离出的c(H+)>0.1mol•L-1NaOH溶液中由水电离出的c(H+);(选填“>”、“<”、或“=”)
(3)求出混合液的下列算式的精确计算结果(填具体数字):
c(Na+)-c (A-)=9.9×10-7mol•L-1;c (HA)=10-8mol•L-1
(4)已知NH4A溶液是中性,又知将HA溶液加入到Na2CO3溶液中有气体放出,试推断
(NH4)2CO3溶液的pH>7 (选填“>”、“<”或“=”);
(5)将相同温度下浓度相同的四种盐溶液:
A.NH4HCO3 B.NH4A C.(NH4)2SO4 D.NH4Cl
按c (NH4+)由大到小的顺序排列A>B>D>C(填序号)
(6)用0.1mol•L-1NaOH溶液分别去中和VmLPH=2的HA溶液与盐酸溶液,消耗NaOH溶液的体积分别为a、b,则a与b的大小关系为:a>b.
分析 (1)盐溶液呈碱性说明该盐能水解导致溶液中氢氧根离子浓度大于氢离子浓度而使溶液呈碱性;
(2)含有弱根离子的盐能促进水电离,酸或碱能抑制水电离;
(3)溶液中存在电荷守恒、质子守恒,根据电荷守恒、质子守恒计算;
(4)根据题意知,HA的酸性比碳酸强,NH4A溶液为中性,说明铵根离子和该酸根离子水解程度相同,由此得知铵根离子水解程度小于碳酸根离子,所以(NH4)2CO3中溶液呈碱性;
(5)根据铵根离子的水解程度判断溶液酸碱性的大小,溶液浓度越稀,盐的水解程度越大;
(6)分别与等浓度的NaOH溶液反应,消耗NaOH溶液体积与酸的浓度成正比.
解答 解:(1)等物质的量的一元酸和一元碱恰好反应生成盐和水,生成的盐溶液呈碱性说明该酸是弱酸,生成的盐能水解导致溶液中氢氧根离子浓度大于氢离子浓度,溶液的pH值大于7,水解方程式为:A-+H2O?HA+OH-,
故答案为:A-+H2O?HA+OH-;
(2)该盐含有弱根离子能促进水电离,氢氧化钠是强碱能抑制水电离,所以混合溶液中由水电离出的c(H+)>0.1mol•L-1NaOH溶液中由水电离出的c(H+),
故答案为:>;
(3)由电荷守恒可知,c(Na+)-c(A-)=c(OH-)-c(H+)=10-6-10-8=9.9×10-7mol/L;根据质子守恒得c(HA)+c(H+)=c(OH-),则c(OH-)-c(HA)=c(H+)=10-8mol/L,
故答案为:9.9×10-7 ;10-8;
(4)将HA溶液加到Na2CO3溶液中有气体放出,说明HA的酸性比碳酸的强,NH4A溶液为中性,说明相同条件下,氨水和HA的电离程度相同,所以(NH4)2CO3中铵根离子的水解程度小于碳酸根离子的水解程度,所以溶液的pH>7;
故答案为:>;
(5)(NH4)2SO4 和NH4Cl是强酸弱碱盐,铵根离子水解导致溶液呈酸性,溶液中铵根离子浓度越大,水解程度越小,但水解的个数多,所以氯化铵溶液的pH值大于硫酸铵;
NH4A溶液中阴阳离子的水解程度相等,所以溶液呈中性,溶液的pH值大于氯化铵;
NH4HCO3溶液中铵根离子的水解程度小于碳酸氢根离子的水解程度,溶液呈碱性,所以溶液的pH值最大,则pH大小顺序为A>B>D>C,
故答案为:A>B>D>C;
(6)分别与等浓度的NaOH溶液反应,消耗NaOH溶液体积与酸的浓度成正比,等pH的HA、HCl,HA的浓度大于盐酸,所以HA消耗的氢氧化钠多,即a>b,
故答案为:a>b.
点评 本题考查了盐溶液呈酸碱性的原因、溶液酸碱性的判断、离子浓度大小的比较等知识点,难度较大,难点是判断相同温度、相同浓度下氯化铵和硫酸铵溶液pH值大小的比较,溶液越稀铵根离子的水解程度越大,但水解的个数少,但氯化铵溶液的pH值大于硫酸铵溶液的pH值.

| A. | 非金属元素间形成的化学键都是共价键 | |
| B. | 第三周期主族元素的最高正化合价等于它所处的族序数 | |
| C. | 短周期元素形成离子后,最外层都达到8电子稳定结构 | |
| D. | 最外层电子数相同的原子属于同一族且化学性质相似 |
根据题意完成下列计算:
(1)某氯碱厂测得某组电解槽的阳极每小时产生气体485.92m3(折算到标准状况,下同),合2.169×104mol;测知其中Cl2的体积分数为0.985(杂质为O2),则该气体的密度为3.144g/L;阴极产生NaOH4.273×104mol(保留四位有效数字,下同).
(2)下表提供了两极溶液浓度的变化数据(阴阳两个极区的物料不流通,忽略其中溶液的体积变化).
| 阴极:NaOH溶液质量分数 | 阳极:NaCl溶液浓度(g/L) | |
| 进料液 | 0.30 | 310 |
| 电解后 | 0.32 | 210 |
(3)产品之一----漂水(NaClO溶液)具有良好的消毒、漂白能力.在制漂水过程中取1L溶液,测得pH=12(忽略水解),NaClO含量为0.3725g.在一定条件下,将该溶液制成晶体,质量最多为1.335g.通过列式计算,写出该晶体的化学式.
【实验原理】2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O
【实验内容及记录】
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 溶液褪至无色所需时间/min | |||
| 0.6mol/L H2C2O4溶液 | H2O | 3mol/L 稀H2SO4溶液 | 0.05mol/L KMnO4溶液 | ||
| 1 | 3.0 | 2.0 | 2.0 | 3.0 | 1.5 |
| 2 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
| 3 | 1.0 | 4.0 | 2.0 | 3.0 | 3.9 |
(1)根据表中的实验数据,可以得到的结论是其他条件不变时,增大(减小)反应物浓度,加快(减慢)化学反应速率.
(2)利用实验1中的数据,计算用KMnO4表示的化学反应速率为1.0×10-2mol/(L•min).
(3)该小组同学根据经验绘制了n(Mn2+)随时间变化的趋势如图1所示,但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的实际趋势如图2所示.
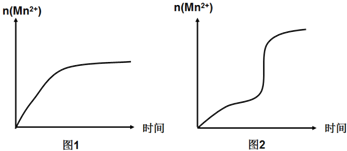
该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究.
①该小组同学提出的假设是Mn2+对该反应有催化作用.
②请你帮助该小组同学完成实验方案,并填写表中空白
| 实验编号 | 室温下,试管中所加试剂及其用量 | 再向试管中加入某种固体 | 溶液褪至无色所需时间/min | |||
| 0.6mol/L H2C2O4溶液 | H2O | 3mol/L 稀H2SO4溶液 | 0.05mol/L KMnO4溶液 | |||
| 4 | 3.0 | 2.0 | 2.0 | 3.0 | MnSO4 | t |
 已知1-丁醇的沸点为117.7℃,乙酸的沸点为118℃,甲同学拟在浓硫酸作用下,使1-丁醇和乙酸进行酯化反应制乙酸丁酯(反应温度115~125℃)
已知1-丁醇的沸点为117.7℃,乙酸的沸点为118℃,甲同学拟在浓硫酸作用下,使1-丁醇和乙酸进行酯化反应制乙酸丁酯(反应温度115~125℃)