题目内容
5.已知某浓度的硫酸在水中的电离方程式:H2SO4═H++HSO4-,HSO4-?H++SO42-.
(1)Na2SO4溶液显碱性(填“酸性”“碱性”或“中性”),理由是(用离子方程式表示)SO42-+H2O?HSO4-+OH-.
(2)在25℃时0.1mol•L-1的NaHSO4溶液中c(SO42-)=0.029mol•L-1,则25℃时,0.1mol•L-1 H2SO4溶液中c(SO42-)小于 0.029mol•L-1(填“大于”,“小于”或“等于”),理由是H2SO4一级电离出H+,对HSO4-电离起抑制作用,而NaHSO4中不存在抑制.
(3)在0.1mol•L-1 Na2SO4溶液中,下列粒子浓度关系正确的是AD.
A.c(Na+)+c(H+)=c(OH-)+c(HSO4-)+2c(SO42-)
B.2c(Na+)=c(SO42-)+c(HSO4-)
C.c(Na+)>c(SO42-)>c(H+)>c(OH-)
D.c(SO42-)+c(HSO4-)=0.1mol•L-1.
分析 (1)硫酸的第一步电离是完全的:H2SO4=H++HSO4-,第二步电离并不完全:HSO4-?H++SO42-,Na2SO4溶液存在SO42-+H2O?OH-+HSO4-;
(2)硫酸第一步电离出的氢离子抑制第二步电离;
(3)硫酸氢离子水解导致溶液呈碱性,溶液中存在电荷守恒和物料守恒,根据电荷守恒和物料守恒判断.
解答 解:(1)根据硫酸的第一步电离是完全的:H2SO4=H++HSO4-,第二步电离并不完全:HSO4-?H++SO42-,则
Na2SO4溶液存在SO42-+H2O?OH-+HSO4-,溶液呈弱碱性,故答案为:碱性;SO42-+H2O?OH-+HSO4-;
(2)硫酸第一步电离出的氢离子抑制第二步电离,所以0.10mol•L-1的H2SO4溶液中c(H+)<0.129mol•L-1,故答案为:小于;H2SO4一级电离出H+,对HSO4-电离起抑制作用,而NaHSO4中不存在抑制;
(3)A.溶液中存在电荷守恒,根据电荷守恒得c(Na+)+c(H+)=c(OH-)+c(HSO4-)+2c(SO42-),故A正确
B.硫酸根离子只发生一步水解,溶液中存在物料守恒,根据物料守恒得c(Na+)=2c(SO42-)+2c(HSO4-),故B错误;
C.硫酸根离子水解导致溶液呈碱性,所以c(OH-)>c(H+),根据物料守恒得c(Na+)>c(SO42-),硫酸根离子水解程度较小,所以离子浓度大小顺序是c(Na+)>c(SO42-)>c(OH-)>c(H+),故C错误;
D.根据物料守恒得c(SO42-)+c(HSO4-)=0.1mol•L-1,故D正确;
故选AD.
点评 本题考查酸碱混合溶液定性判断及弱电解质电离、盐类水解等知识点,侧重考查学生分析能力,把握硫酸电离特点是解本题关键,注意硫酸第一步完全电离、第二步部分电离,所以硫酸根离子只有一步水解,为易错题.

| A. | 含等物质的量的NaHC2O4和Na2C2O4的溶液:3c(Na+)═2[c(HC2O4-)+c(C2O42-)+c(H2C2O4)] | |
| B. | 等pH的氨水、KOH溶液、Ba(OH)2溶液中:c(NH4+)=c(K+)=c(Ba2+) | |
| C. | 加水稀释CH3COONa溶液,溶液中$\frac{c(C{H}_{3}COOH)c(O{H}^{-})}{c(C{H}_{3}CO{O}^{-})}$的值变小 | |
| D. | 25℃时,pH=4的盐酸与pH=4的醋酸溶液等体积混合后pH=4 |
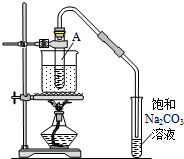 按如图所示装置,在试管A里加入3mL乙醇和2mL冰醋酸,然后一边摇动,一边慢慢地加入2mL浓硫酸,再加入少量碎瓷片,用酒精灯加热10min,结果在饱和碳酸钠溶液的液面上没有无色油状液体,下列对其原因的分析错误的是( )
按如图所示装置,在试管A里加入3mL乙醇和2mL冰醋酸,然后一边摇动,一边慢慢地加入2mL浓硫酸,再加入少量碎瓷片,用酒精灯加热10min,结果在饱和碳酸钠溶液的液面上没有无色油状液体,下列对其原因的分析错误的是( )| A. | 试管A中没有发生反应 | |
| B. | 热源小、水量多,水浴升温速度太慢 | |
| C. | 产物蒸汽在试管A上部全部被冷凝回流 | |
| D. | 产物已全部溶解在饱和Na2CO3溶液中 |
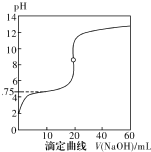 25℃时,用0.1000mol•L-1NaOH溶液滴定20mL0.1000mol•L-1一元酸HA(pKa=-lgKa=4.75)溶液,其滴定曲线如右图所示.下列说法正确的是( )
25℃时,用0.1000mol•L-1NaOH溶液滴定20mL0.1000mol•L-1一元酸HA(pKa=-lgKa=4.75)溶液,其滴定曲线如右图所示.下列说法正确的是( )| A. | 当滴人40mLNaOH溶液时,溶液中:c(Na+)>c(A-)>c(OH-)>c(H+) | |
| B. | 当溶液中c(H+)+c(OH-)=2×10-7时:c(Na+)>c(A-)>c(OH-)=c(H+) | |
| C. | 当滴人NaOH溶液20mL时c(OH-)>c(H+)+c(HA) | |
| D. | 当滴定到pH=4.75时,c(A-)=c(HA) |
| A. | pH=2的HA溶液与pH=12的MOH溶液任意比混合:c(H+)+c(M+)=c(OH-)+c(A-) | |
| B. | B氨水和盐酸混合后溶液呈酸性,溶液中可能存在:c(NH4+)>c(Cl-) | |
| C. | 在一定温度下,相同pH的硫酸和硫酸铁溶液中水电离出来的c(H+)分别是1.0×0×10-amol/L和是1.0×10-bmol/L,在此温度时,水的离子积为1.0×10-(a+b) | |
| D. | 常温下,0.1mol/L酸HA pH=3,0.1mol/L 碱BOH pH=13,则盐BA溶液的pH<7 |
| 酸 | 电离方程式 | 电离常数 K/mol•L-1 |
| CH3COOH | CH3COOH?CH3COO-+H+ | 1.26×10-5 |
| H2CO3 | H2CO3?H++HCO3- HCO3-?CO32-+H+ | K1=4.31×10-7 K2=5.61×10-11 |
| H2S | H2S?H++HS- HS-?H++S2- | K1=9.1×10-8 K2=1.1×10-12 |
| H3PO4 | H3PO4?H++H2PO4- H2PO4-?H++HPO42- HPO42-?H++PO43- | K1=7.52×10-3 K2=6.23×10-8 K3=2.20×10-13 |
(1)K只与温度有关,当温度升高时,K值增大(填“增大”、“减小”或“不变”).
(2)在温度相同时,各弱酸的K值不同,那么K值的大小与酸性的相对强弱有何关系?K值越大,电离程度越大,酸性越强;
(3)若把CH3COOH、H2CO3、HCO3-、H2S、HS-、H3PO4、H2PO4-、HPO42-都看作是酸,其中酸性最强的是H3PO4,最弱的是HPO42-;
(4)H3PO4的Ka1、Ka2、Ka3之间存在数量上的规律,此规律是在数值上相差很大,产生此规律的原因是上一级电离产生的H+对下一级电离有抑制作用.
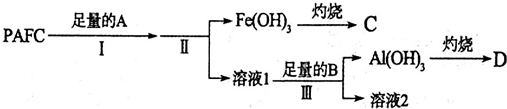
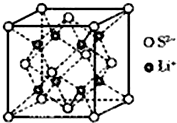 硫的单质及其化合物在工农业生产中的用途非常广泛.回答下列问题:
硫的单质及其化合物在工农业生产中的用途非常广泛.回答下列问题: )易溶于CS2,固态时属于分子晶体,其中硫原子杂化轨道类型为sp3.
)易溶于CS2,固态时属于分子晶体,其中硫原子杂化轨道类型为sp3. ).
).