题目内容
2.一定条件下,向一容积固定的密闭容器中通入2mol SO2和1mol O2,发生2SO2+O2?2SO3△H<0,一段时间后达到平衡,SO2、O2、SO3的物质的量分别为a mol、b mol、c mol,按要求回答下列问题.(1)平衡后,通入2mol SO2,则SO2的转化率减小,O2的转化率增大.(填“增大”、“减小”或“不变”,下同).
(2)平衡后,通入2mol SO2,1mol O2,则SO2的转化率增大,O2的转化率增大,SO2的百分含量减小,O2的百分含量减小,SO3的百分含量增大.
(3)平衡后,通入a mol SO2,b mol O2,c mol SO3,则SO2的转化率增大,O2的转化率增大,SO2的百分含量减小,O2的百分含量减小,SO3的百分含量增大.
分析 (1)平衡后,通入2mol SO2,二氧化硫浓度增大,平衡正向移动;
(2)平衡后,通入2mol SO2,1mol O2,相当于在原来基础上增大压强,平衡正向移动;
(3)平衡后,通入a mol SO2,b mol O2,c mol SO3,相当于在原来基础上增大压强,平衡正向移动.
解答 解:(1)平衡后,通入2mol SO2,二氧化硫浓度增大,平衡正向移动,SO2的转化率减小,O2的转化率增大,故答案为:减小;增大;
(2)平衡后,通入2mol SO2,1mol O2,相当于在原来基础上增大压强,平衡正向移动,则SO2的转化率增大,O2的转化率 增大,SO2的百分含量 减小,O2的百分含量减小,SO3的百分含量增大,故答案为:增大;增大;减小;减小;增大;
(3)平衡后,通入a mol SO2,b mol O2,c mol SO3,相当于在原来基础上增大压强,平衡正向移动,则SO2的转化率 增大,O2的转化率 增大,SO2的百分含量减小,O2的百分含量减小,SO3的百分含量增大.故答案为:增大;增大;减小;减小;增大.
点评 本题考查化学平衡的移动,为高频考点,把握压强、浓度对平衡移动的影响为解答本题的关键,侧重分析与应用的考查,注意平衡移动原理的应用,题目难度不大.

练习册系列答案
相关题目
12.下列说法中正确的是( )
| A. | 在化合物CaCl2中,除了有Ca2+与Cl-之间的离子键外,还有两个Cl-之间的共价键 | |
| B. | 碘受热升华时共价键被破坏 | |
| C. | 熔化状态下能导电的化合物中一定存在离子键 | |
| D. | 离子化合物中可能含有共价键,共价化合物中可能含有离子键 |
13.下列有水参加的反应中,属于氧化还原反应,且水中有元素被氧化的是( )
| A. | 2Na+2H2O=2NaOH+H2↑ | B. | CaO+H2O═Ca(OH)2 | ||
| C. | SO3+H2O═H2SO4 | D. | 2F2+2H2O═4HF+O2 |
10.25°C时,将两个Pt电极插入一定量的饱和Na2SO4溶液中进行电解,通电一段时间后,在阳极收集到a mol气体,同时有b g Na2SO4•10H2O晶体析出,若保持温度不变,则剩余的Na2SO4溶液的质量分数为( )
| A. | $\frac{71b}{161(b+36a)}$×100% | B. | $\frac{71}{161}$×100% | ||
| C. | $\frac{b}{b+36a}$×100% | D. | $\frac{71b}{161(b+18a)}$×100% |
7.下列叙述正确的是( )
①铁能被磁铁吸引 ②在人体的血红蛋白中含有铁元素
③镁在空气中可剧烈燃烧,并发出强光 ④铁能在氧气中剧烈燃烧,生成黑色的Fe3O4
⑤在空气中加热Cu可生成黑色CuO.
①铁能被磁铁吸引 ②在人体的血红蛋白中含有铁元素
③镁在空气中可剧烈燃烧,并发出强光 ④铁能在氧气中剧烈燃烧,生成黑色的Fe3O4
⑤在空气中加热Cu可生成黑色CuO.
| A. | ①②④⑤ | B. | ②③④⑤ | C. | ①③④⑤ | D. | ①②③④⑤ |
14.下列各操作中,不发生“先产生沉淀,然后沉淀又溶解”现象的是( )
①向石灰水中通入过量的CO2
②向Ca(ClO)2溶液中通入过量SO2
③向氢氧化铝胶体中逐滴滴入过量稀NaOH溶液
④向氯化钡溶液中逐渐通入过量二氧化碳
⑤向AgNO3溶液中逐滴滴入过量稀氨水
⑥向饱和碳酸钠溶液中逐渐通入过量二氧化碳.
①向石灰水中通入过量的CO2
②向Ca(ClO)2溶液中通入过量SO2
③向氢氧化铝胶体中逐滴滴入过量稀NaOH溶液
④向氯化钡溶液中逐渐通入过量二氧化碳
⑤向AgNO3溶液中逐滴滴入过量稀氨水
⑥向饱和碳酸钠溶液中逐渐通入过量二氧化碳.
| A. | ①②⑥ | B. | ①③⑤ | C. | ②④⑥ | D. | ③④⑤ |
11.已知某400mL待测液中可能含有Cl-、SO42-、CO32-、Fe3+和Na+五种离子中的若干种.取该溶液100mL,加入足量NaOH溶液产生红褐色沉淀,过滤、洗涤、灼烧得到1.6g固体,向上述溶液中加足量BaCl2溶液,得到4.66g沉淀,加入盐酸,沉淀不溶解.下列判断不正确的是( )
| A. | 待测液中一定存在SO42-、Fe3+、Cl-,可能存在Na+ | |
| B. | 待测液中:c(Cl-)≥0.2mol•L-1 | |
| C. | 另取100mL待测液加入足量Ba(OH)2溶液,可得6.8g沉淀 | |
| D. | 另取100mL待测液加入足量AgNO3溶液,可得2.87g沉淀 |
15.O3不仅有强氧化性,而且在大气中还具有吸收紫外线的功能,下列关于4.8g O3的说法不正确的是(NA表示阿伏加德罗常数)( )
| A. | 含有原子个数为0.3NA | B. | 分子个数约为6.02×1022 | ||
| C. | 物质的量是0.2mol | D. | 与质量相等的O2所含原子数相等 |
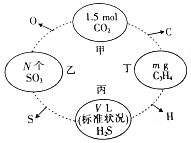 如图,两相邻圆圈内物质间含有相同的某一原子,且该原子的物质的量相同.(设NA为阿伏伽德罗常数的值)
如图,两相邻圆圈内物质间含有相同的某一原子,且该原子的物质的量相同.(设NA为阿伏伽德罗常数的值)