题目内容
15.某化合物的结构式(键线式)及球棍模型如下: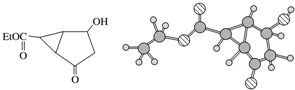
下列关于该有机物的叙述正确的是( )
| A. | 该有机物不同化学环境的氢原子有8种 | |
| B. | 该有机物属于芳香族化合物 | |
| C. | 键线式中的Et代表的基团为-CH3 | |
| D. | 该有机物的分子式为C9H10O4 |
分析 A.该有机物结构不对称,含8种位置的H原子;
B.含有苯环的有机物属于芳香族化合物;
C.Et代表-CH2CH3;
D.由模型可知分子中原子个数.
解答 解:A.该有机物结构不对称,核磁共振波谱图中有8种峰,含8种位置的H原子,故A正确;
B.该有机物中不含苯环,则不属于芳香族化合物,故B错误;
C.由结构及球棍模型可知,Et代表-CH2CH3,故C错误;
D.由1个分子中含9个C原子、12个H原子、4个O原子可知分子式为C9H12O4,故D错误;
故选A.
点评 本题考查有机物的结构与性质,为高频考点,侧重于有机物知识的综合应用,注意把握有机物的结构特点和官能团的性质为解答该题的关键,题目难度不大.

练习册系列答案
相关题目
5.为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行以下五项操作:①过滤;②加过量NaOH溶液;③加适量稀盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液,正确的是( )
| A. | ⑤②④①③ | B. | ④①②⑤③ | C. | ①④②⑤③ | D. | ②④⑤①③ |
6.下列有关化学键的叙述,正确是的( )
| A. | 离子化合物中一定含有离子键 | |
| B. | 单质分子中均不存在化学键 | |
| C. | 含活泼金属元素的化合物一定不是共价化合 | |
| D. | 含有共价键的化合物一定是共价化合物 |
10.下列各组物质中属于同分异构体的是( )
| A. | 葡萄糖和果糖 | B. | 甲烷和乙烷 | C. | 16O和18O | D. | 淀粉和纤维素 |
20.化学在生产和日常生活中有着重要的应用.下列叙述正确的是( )
| A. | 钢铁设备与直流电源正极相连可防腐 | |
| B. | 明矾水解时产生具有吸附性的胶体粒子,可以用于饮用水的杀菌消毒 | |
| C. | 开启啤酒瓶后,瓶中立刻泛起大量泡沫不能用勒夏特列原理解释 | |
| D. | 废旧电池中的汞、锅、铅等重金属盐对土壤和水源会造成污染 |
7.元素周期表是学习化学的重要工具,它隐含着周期表中所反映的许多信息和规律.下表所列是五种短周期的原子半径及主要化合价
(1)用元素代号标出它们在周期表中对应位置(以下为周期表的一部分).
(2)B元素处于周期表中三周期ⅢA族;
(3)在元素周期表中金属与非金属的分界处,可以找到制半导体材料的元素;
(4)上述五种元素的最高价氧化物对应水化物酸性最强的是HClO4(填化学式);
(5)用电子式表示A、D形成化合物的过程 ;
;
(6)C、E形成化合物为SO2、SO3(填化学式).
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | -1 | -2 |
(3)在元素周期表中金属与非金属的分界处,可以找到制半导体材料的元素;
(4)上述五种元素的最高价氧化物对应水化物酸性最强的是HClO4(填化学式);
(5)用电子式表示A、D形成化合物的过程
 ;
;(6)C、E形成化合物为SO2、SO3(填化学式).
5.下列各组物质中,互为同系物的是( )
| A. | CH2=CHCH2CH3和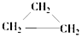 | B. |  和 和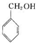 | ||
| C. | 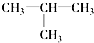 和CH3CH2CH2CH3 和CH3CH2CH2CH3 | D. | CH3CH2Cl与CH3CH2CH2Cl |
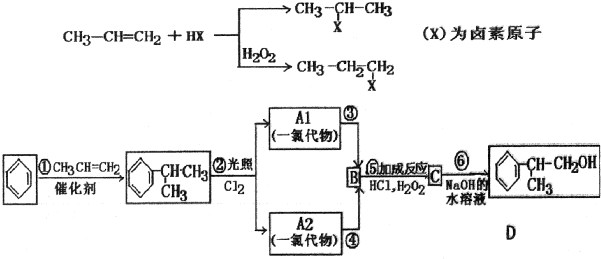
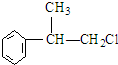 、,
、,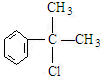 ;
; ,C的结构简式:
,C的结构简式: ;
; +NaCl;
+NaCl;