题目内容
7.元素周期表是学习化学的重要工具,它隐含着周期表中所反映的许多信息和规律.下表所列是五种短周期的原子半径及主要化合价| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | -1 | -2 |
(3)在元素周期表中金属与非金属的分界处,可以找到制半导体材料的元素;
(4)上述五种元素的最高价氧化物对应水化物酸性最强的是HClO4(填化学式);
(5)用电子式表示A、D形成化合物的过程
 ;
;(6)C、E形成化合物为SO2、SO3(填化学式).
分析 C、E都有-2价,处于ⅥA族,且C有+6价、原子半径较大,故C为S元素、E为O元素;D元素有-1价,原子半径大于氧,故D为Cl;A有+2价,处于ⅡA族,B有+3价,处于ⅢA族,且原子半径A>B>硫,故A为Mg、B为Al元素.
解答 解:C、E都有-2价,处于ⅥA族,且C有+6价、原子半径较大,故C为S元素、E为O元素;D元素有-1价,原子半径大于氧,故D为Cl;A有+2价,处于ⅡA族,B有+3价,处于ⅢA族,且原子半径A>B>硫,故A为Mg、B为Al元素.
(1)用元素代号标出它们在周期表中对应位置:
| E | |||||||||||||||||
| A | B | C | D | ||||||||||||||
故答案为:
| E | |||||||||||||||||
| A | B | C | D | ||||||||||||||
(2)B元素处于周期表中第三周期ⅢA族,故答案为:三、ⅢA;
(3)在元素周期表中金属与非金属的分界处,可以找到制半导体材料的元素,故答案为:金属与非金属;
(4)上述五种元素的最高价氧化物对应水化物酸性最强的是HClO4,故答案为:HClO4;
(5)A、D形成化合物为MgCl2,用电子式表示形成过程:
 ,
,故答案为:
 ;
;(6)C、E形成化合物为:SO2、SO3,故答案为:SO2、SO3.
点评 本题考查结构性质位置关系应用,根据化合价与原子半径推断元素是解题关键,注意元素周期律的理解掌握,难度不大.

练习册系列答案
相关题目
17.下表中,对有关除杂的方法不正确的是( )
| 选项 | 物质 | 杂质 | 方法 |
| A | 苯 | 苯酚 | 加浓溴水后过滤 |
| B | 苯 | 甲苯 | 依次加入酸性高锰酸钾溶液、NaOH溶液后分液 |
| C | 溴苯 | Br2 | 加NaOH溶液后分液 |
| D | 乙酸乙酯 | 乙酸 | 加饱和碳酸钠溶液后分液 |
| A. | A | B. | B | C. | C | D. | D |
18.不能证明HA是弱酸的是( )
| A. | 0.01 mol•L-1HA溶液的pH=4 | B. | HA溶液跟锌反应,放出H2很慢 | ||
| C. | pH=2的HA溶液稀释100倍后pH=3.5 | D. | 溶液中存在HA的电离平衡 |
15.某化合物的结构式(键线式)及球棍模型如下:
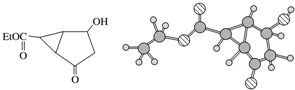
下列关于该有机物的叙述正确的是( )

下列关于该有机物的叙述正确的是( )
| A. | 该有机物不同化学环境的氢原子有8种 | |
| B. | 该有机物属于芳香族化合物 | |
| C. | 键线式中的Et代表的基团为-CH3 | |
| D. | 该有机物的分子式为C9H10O4 |
2.相同温度下,相同物质的量浓度的四种溶液:①CH3COONa,②NaHSO4,③NaCl,④ .按pH值由大到小顺序排列正确的是( )
.按pH值由大到小顺序排列正确的是( )
 .按pH值由大到小顺序排列正确的是( )
.按pH值由大到小顺序排列正确的是( )| A. | ④①③② | B. | ①④③② | C. | ①②③④ | D. | ④③②① |
16.14g 铁粉全部溶于某稀硝酸中,恰好反应,放出 NO 气体后得到溶液 1L.称量所得溶液,发现比原硝酸溶液增重 8g.则原溶液中硝酸的浓度为( )
| A. | 0.4 mol/L | B. | 0.6 mol/L | C. | 0.8 mol/L | D. | 1.0 mol/L |