题目内容
在0.2L由NaCl、MgCl2、BaCl2组成的混合液中,部分离子浓度大小如右图所示,回答下列问题:

(1)该混合液中含溶质NaCl的物质的量为_________mol,含溶质MgCl2的质量为__________g。
(2)该混合液中含溶质MgCl2的物质的量为____________,将该混合液加水稀释至体积为1L,稀释后溶液中Ba2+的物质的量浓度为_________mol/L
(3)若向该混合液溶液中通入NH3使Mg2+完全沉淀,需要标况下NH3_____________L。
已知MgCl2+2NH3=Mg(OH)2↓+2NH4Cl
练习册系列答案
相关题目
700 ℃时,向容积为2 L的密闭容器中充入一定量的CO和H2O,发生反应:
CO(g)+H2O(g)  CO2(g)+H2(g)
CO2(g)+H2(g)
反应过程中测定的部分数据见下表(表中t2>t1):
反应时间/min | n(CO)/mol | n(H2O)/mol |
0 | 1.20 | 0.60 |
t1 | 0.80 | |
t2 | 0.20 |
 下列说法正确的是( )
下列说法正确的是( )
A.反应在t1 min内的平 均速率为:v(H2)=
均速率为:v(H2)=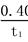 mol·L-1·min-1
mol·L-1·min-1
B.保持其他条件不变,起始时向容器中充入0.60 mol CO和1.20 mol H2O,达到平衡时n(CO2)=0.40 mol
C.保持其他条件不变,向平衡体系中再通入0.20 mol H2O,与原平衡相比,达到新平衡时CO转化率不变,H2O的体积分数不变
D.温度升高至800 ℃,上述反应平衡常数为0.64,则正反应为吸热反应



 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH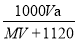 B.
B.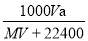 C.
C. D.
D.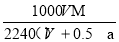
 C(g)+2 D(g)(a为正整数)。反应过程中,当其他条件不变时,C的百分含量(C%)与
C(g)+2 D(g)(a为正整数)。反应过程中,当其他条件不变时,C的百分含量(C%)与 温度(T)和压强(p)的关系如图所示。下列说法不正确的是
温度(T)和压强(p)的关系如图所示。下列说法不正确的是