题目内容
7.选择下列实验方法分离物质,将分离方法的序号填在横线上:A.过滤 B.结晶 C.分液 D.蒸馏 E.萃取分液
①C 分离水和植物油的混合物;
②A 分离饱和氯化钾溶液和沙子的混合物;
③B 从硝酸钾和氯化钠的混合溶液中获得硝酸钾;
④D 分离酒精(沸点为78.1℃)和甲苯(沸点为110.6℃)的混合物;
⑤E 将碘水中的碘单质与水分离.
分析 ①水和植物油分层;
②沙子不溶于水;
③硝酸钾和氯化钠的溶解度受温度影响不同;
④酒精与甲苯互溶,但沸点不同;
⑤碘不易溶于水,易溶于有机溶剂.
解答 解:①水和植物油分层,则选择分液法分离,故答案为:C;
②沙子不溶于水,则选择过滤法分离,故答案为:A;
③硝酸钾和氯化钠的溶解度受温度影响不同,则选择结晶法分离,故答案为:B;
④酒精与甲苯互溶,但沸点不同,则选择蒸馏法分离,故答案为:D;
⑤碘不易溶于水,易溶于有机溶剂,则选择萃取分液法分离,故答案为:E.
点评 本题考查混合物分离提纯,为高频考点,把握物质性质、性质差异、混合物分离方法为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案
相关题目
17.在25℃、101kPa下,0.1mol甲醇燃烧生成CO2和液态水时放热72.65kJ,下列热化学方程式正确的是( )
| A. | CH3OH (l)+$\frac{3}{2}$O2 (g)═CO2(g)+2H2O(l)△H=+726.5 kJ/mol | |
| B. | 2CH3OH (l)+3O2 (g)═2CO2(g)+4H2O(g)△H=+1453 kJ/mol | |
| C. | CH3OH (l)+$\frac{3}{2}$O2 (g)═CO2(g)+2H2O(l)△H=-726.5 kJ/mol | |
| D. | 2CH3OH (l)+3O2 (g)═2CO2(g)+4H2O(g)△H=-1453 kJ/mol |
18.对于反应4CO(g)+2NO2(g)═N2(g)+4CO2(g),以下化学反应速率的表示中,所表示反应速率最快的是( )
| A. | v(CO)=1.6 mol•(L•min)-1 | B. | v(NO2)=0.9 mol•(L•min)-1 | ||
| C. | v(N2)=0.25mol•(L•min)-1 | D. | v(CO2)=1.2 mol•(L•min)-1 |
2.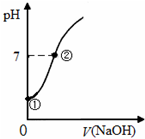 常温下,向饱和氯水中逐滴滴入0.1mol•L-1的氢氧化钠溶液,pH变化如图所示,下列有关叙述正确的是( )
常温下,向饱和氯水中逐滴滴入0.1mol•L-1的氢氧化钠溶液,pH变化如图所示,下列有关叙述正确的是( )
 常温下,向饱和氯水中逐滴滴入0.1mol•L-1的氢氧化钠溶液,pH变化如图所示,下列有关叙述正确的是( )
常温下,向饱和氯水中逐滴滴入0.1mol•L-1的氢氧化钠溶液,pH变化如图所示,下列有关叙述正确的是( )| A. | ①点所示溶液中只存在HClO的电离平衡 | |
| B. | ①到②水的电离程度逐渐减小 | |
| C. | I-能在②点所示溶液中存在 | |
| D. | ②点所示溶液中:c(Na+)=c(Cl-)+c(ClO-) |
12.下列过程中,需吸收能量的是( )
| A. | H+H→H2 | B. | 天然气燃烧 | C. | I2→I+I | D. | S+O2→SO2 |
19.常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如表:
请回答:
(1)从a组情况分析,HA是强酸还是弱酸HA是弱酸.
(2)b组情况表明,c>0.2 (选填“>”、“<”或“=”).混合溶液中离子浓度c(A-)= c(Na+).(选填“>”、“<”或“=”)
(3)a组实验所得混合溶液中由水电离出的c(OH-)=10-5 mol•L-1.
| 实验编号 | HA物质的量浓度(mol•L-1) | NaOH物质的量浓度(mol•L-1) | 混合溶液的pH |
| a | 0.1 | 0.1 | pH=9 |
| b | c | 0.2 | pH=7 |
(1)从a组情况分析,HA是强酸还是弱酸HA是弱酸.
(2)b组情况表明,c>0.2 (选填“>”、“<”或“=”).混合溶液中离子浓度c(A-)= c(Na+).(选填“>”、“<”或“=”)
(3)a组实验所得混合溶液中由水电离出的c(OH-)=10-5 mol•L-1.
16.下列有关实验现象的描述中,正确的是( )
| A. | 氢气在氯气中剧烈燃烧,产生苍白色火焰,有白雾生成 | |
| B. | 铁在氯气中剧烈燃烧,生成蓝色的氯化铁颗粒 | |
| C. | 过氧化钠投入水中,会产生气泡 | |
| D. | 钠在空气中剧烈燃烧,得到白色粉末状固体 |
17.下列离子方程式不正确的是( )
| A. | NaNO2溶液中加入酸性KMnO4溶液:2MnO4-+5NO2-+6H+═2Mn2++5NO3-+3H2O | |
| B. | 0.5mol/L的NaHSO3溶液与1.0mol/L的NaClO溶液等体积混合:HSO3-+2ClO-=SO42-+Cl-+HClO | |
| C. | Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-═2Fe2++I2 | |
| D. | NH4HSO4的稀溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全:NH4++H++SO42-+Ba2++2OH-=NH3?H2O+BaSO4↓+H2O |
 .
.