题目内容
常温下a mol/L CH3COOH稀溶液和b mol/L KOH稀溶液等体积混合,下列判断一定正确的是( )
| A、若c(OH-)>c(H+),a=b |
| B、若c(K+)>c(CH3COO-),a>b |
| C、若c(OH-)=c(H+),a>b |
| D、若c(K+)<c(CH3COO-),a<b |
考点:酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:A、若c(OH-)>c(H+),则溶液显示碱性,溶液组成可以是醋酸钾和氢氧化钾的混合物还可以是醋酸钾的溶液;
B、若c(K+)>c(CH3COO-),根据电荷守恒,则c(OH-)>c(H+),溶液组成可以是醋酸钾和氢氧化钾的混合物还可以是醋酸钾的溶液;
C、若c(OH-)=c(H+),溶液显示中性;
D、若c(K+)<c(CH3COO-),则c(OH-)<c(H+),溶液显示酸性,溶液组成是醋酸钾和醋酸的混合物.
B、若c(K+)>c(CH3COO-),根据电荷守恒,则c(OH-)>c(H+),溶液组成可以是醋酸钾和氢氧化钾的混合物还可以是醋酸钾的溶液;
C、若c(OH-)=c(H+),溶液显示中性;
D、若c(K+)<c(CH3COO-),则c(OH-)<c(H+),溶液显示酸性,溶液组成是醋酸钾和醋酸的混合物.
解答:
解:A、若c(OH-)>c(H+),则溶液显示碱性,溶液组成可以是醋酸钾和氢氧化钾的混合物还可以是醋酸钾的溶液,所以可以是a≤b,故A错误;
B、若c(K+)>c(CH3COO-),根据电荷守恒,则c(OH-)>c(H+),溶液组成可以是醋酸钾和氢氧化钾的混合物还可以是醋酸钾的溶液,所以可以是a≤b,故A错误;
C、若c(OH-)=c(H+),溶液显示中性,溶液组成是醋酸钾和醋酸的混合物,所以a>b,故C正确;
D、若c(K+)<c(CH3COO-),则c(OH-)<c(H+),溶液显示酸性,溶液组成是醋酸钾和醋酸的混合物,所以a>b,故D错误.
故选C.
B、若c(K+)>c(CH3COO-),根据电荷守恒,则c(OH-)>c(H+),溶液组成可以是醋酸钾和氢氧化钾的混合物还可以是醋酸钾的溶液,所以可以是a≤b,故A错误;
C、若c(OH-)=c(H+),溶液显示中性,溶液组成是醋酸钾和醋酸的混合物,所以a>b,故C正确;
D、若c(K+)<c(CH3COO-),则c(OH-)<c(H+),溶液显示酸性,溶液组成是醋酸钾和醋酸的混合物,所以a>b,故D错误.
故选C.
点评:本题考查学生盐的水解原理和实质,注意知识的积累是解题的关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
短周期元素X、Y、Z、W的原子序数依次增大,且原子最外层电子数之和为13.X的原子半径比Y的小,X与W同主族,Z原子的最外层电子数是其内层电子数的3倍.下列说法正确的是( )
| A、元素Z、W的简单离子的电子层结构不同 |
| B、元素的非金属性由强到弱:Y>Z>X |
| C、只含X、Y、Z 三种元素的化合物,可能是离子化合物,也可能是共价化合物 |
| D、元素Y的气态氢化物与其最高价氧化物对应的水化物不反应 |
标准状况下,密闭容器内分别充入空气和H2、O2的混合气体在可移动的活塞两边,充入时体积如图所示,若将装置右边H2、O2的混合气体点燃引爆,活塞先左弹,恢复至原温度后,活塞右滑最终停在容器的正中央,则原来H2、O2的体积比最接近于( )
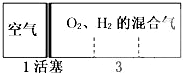
①2:7 ②5:4 ③4:5 ④7:2.
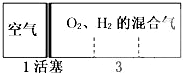
①2:7 ②5:4 ③4:5 ④7:2.
| A、①② | B、②④ | C、③④ | D、①③ |
已知短周期元素的离子.aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
| A、原子半径 A>B>D>C |
| B、a-c=1 |
| C、离子半径 C>D>B>A |
| D、单质的还原性 A>B>D>C |
下列有关钠、铁、铝性质的说法中不正确的是( )
| A、钠、铝均能从FeCl3溶液中置换出铁单质 |
| B、均能与盐酸反应,但金属钠与盐酸的反应最剧烈 |
| C、在地壳中的含量:Al>Fe>Na |
| D、钠、铝均能与NaOH溶液反应,但参加反应的物质种类前者少于后者 |
下列离子方程式书写不正确的是:( )
| A、碳酸钠溶液中加酚酞显红色:CO32-+H2O?HCO3-+OH- |
| B、用醋酸除去水垢(主要成分是碳酸钙):CaCO3+2H+ Ca2++H2O+CO2↑ |
| C、稀硫酸与小苏打溶液反应:H++HCO3-H2O+CO2↑ |
| D、氢氧化铁溶于氢碘酸:2Fe(OH)3+6H++2I-2Fe2++I2+6H2O |
