题目内容
 按照如图装置持续通入X气体或蒸气,可以看到a处有红色物质生成,b处变蓝,c处得到液体,则X气体或蒸气可能是(假设每个反应均完全)( )
按照如图装置持续通入X气体或蒸气,可以看到a处有红色物质生成,b处变蓝,c处得到液体,则X气体或蒸气可能是(假设每个反应均完全)( )| A、CH3CH2OH |
| B、CO或H2 |
| C、NH3 |
| D、C(CH3)3(OH) |
考点:实验装置综合
专题:实验题
分析:持续通入X气体,可以看到a处有红色物质生成,说明CuO被还原生成Cu,b处变蓝,说明有水生成,结合c处得到液体以及题给物质的性质解答该题.
解答:
解:A.CH3CH2OH与CuO发生CH3CH2OH+CuO
CH3CHO+H2O+Cu,可观察到a处有红色物质生成,b处变蓝,c处得到有刺激性气味的液体乙醛,故A正确;
B.CO与CuO反应生成CO2,不能使b处变蓝,故B错误;
C.NH3与CuO反应生成Cu、N2和H2O,可以看到a处有红色物质生成,b处变蓝,但在c出不能得到液体,故C错误;
D.C(CH3)3(OH)不能被CuO氧化,故D错误.
故选A.
| △ |
B.CO与CuO反应生成CO2,不能使b处变蓝,故B错误;
C.NH3与CuO反应生成Cu、N2和H2O,可以看到a处有红色物质生成,b处变蓝,但在c出不能得到液体,故C错误;
D.C(CH3)3(OH)不能被CuO氧化,故D错误.
故选A.
点评:本题考查实验装置综合及物质的性质,为高频考点,侧重于学生的分析能力和实验能力的考查,掌握醇的催化氧化的反应原理是解答的关键,答题时注意把握题给信息,题目难度中等,选项D为解答的难点.

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案
相关题目
A、B、C、D是短周期元素,在周期表中有如图的位置关系,下列分析不正确的是( )
| A | B |
| C | D |
| A、若D是双原子分子,则单质的熔点大小关系为D>B>A |
| B、若C单质为原子晶体,且具有金属光泽.则B的氢化物分子式为BH3 |
| C、若A元素原子最外层只有1个电子,则D单质既能与酸又能与碱溶液反应 |
| D、A和C可形成CA3型化合物,则一定能形成CA2型化合物 |
锌与很稀的硝酸反应4Zn+10HNO3=4Zn(NO3)3+NH4NO3+3H2O,当生成1mol硝酸锌时被还原的硝酸的物质的量为( )
| A、2.5mol |
| B、1mol |
| C、0.5mol |
| D、0.25mol |
若ABn的中心原子A上没有孤对电子,运用价层电子对互斥模型,下列说法正确的是( )
| A、若n=2,则分子的立体结构为V形 |
| B、若n=3,则分子的立体结构为三角锥形 |
| C、若n=4,则分子的立体结构为正四面体形 |
| D、以上说法都不正确 |
下列说法正确的是( )
| A、某钾盐溶于盐酸,产生无色无味的气体,将气体通入澄清石灰水,有白色沉淀生成,则该钾盐一定是K2CO3 |
| B、取试剂少量于试管,滴加入少量BaCl2溶液,生成白色沉淀,加稀HNO3白色沉淀不溶解,证明该试剂中一定含SO42- |
| C、用某盐做焰色反应,火焰为黄色,说明该盐一定含Na+,一定不含K+ |
| D、取黄色溶液少量于试管,滴加KSCN(aq),呈红色,该溶液中一定含有Fe3+ |
某溶液由相同物质的量的CuCl2、FeCl3、AlCl3混合而成,向该溶液中加入铁粉,充分搅拌后振荡,铁粉仍有剩余,则溶液中存在较多的阳离子是( )
| A、Fe2+、Al3+ |
| B、Fe2+、Fe3+ |
| C、Fe3+、Al3+ |
| D、Fe2+、Cu2+ |
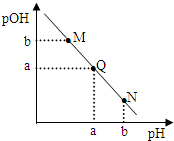 某温度下,向一定体积的0.1mol/L的醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH与pH的关系如图[已知:pOH=-lgc(OH-)],下列说法正确的是
某温度下,向一定体积的0.1mol/L的醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH与pH的关系如图[已知:pOH=-lgc(OH-)],下列说法正确的是( )
| A、M点溶液导电能力强于Q点溶液导电能力 |
| B、N点所示溶液中,c(CH3COO-)>c(Na+) |
| C、M点与N点所示溶液中水的电离程度相等 |
| D、Q点消耗NaOH溶液体积等于醋酸溶液的体积 |
