题目内容
氢氧化铁胶体与氯化铁溶液,具有的共同性质是( )
| A、能透过半透膜 |
| B、分散质颗粒直径都在1~100mm之间 |
| C、呈红褐色 |
| D、加热蒸干、灼烧后都有氧化铁生成 |
考点:胶体的重要性质
专题:
分析:根据溶液和胶体的性质和铁盐的性质作答,
A、胶粒不能透过半透膜;
B、根据溶液和胶体粒子半径大小不同,直径范围不一样;
C、氯化铁溶液是黄色的液体;
D、氯化铁中铁水解生成氢氧化铁,氢氧化铁加热得到氧化铁.
A、胶粒不能透过半透膜;
B、根据溶液和胶体粒子半径大小不同,直径范围不一样;
C、氯化铁溶液是黄色的液体;
D、氯化铁中铁水解生成氢氧化铁,氢氧化铁加热得到氧化铁.
解答:
解:A、溶液能透过半透膜,胶粒不能透过半透膜,故A错误;
B、溶液中溶质粒子直径较小于1nm,胶体粒子直径在l~100nm之间,故B错误;
C、氯化铁溶液是黄色的液体,氢氧化铁胶体呈红褐色,故C错误;
D、氢氧化铁胶体加热得到氧化铁,氯化铁溶液中铁水解生成氢氧化铁,加热生成氧化铁,故D正确;
故选:D.
B、溶液中溶质粒子直径较小于1nm,胶体粒子直径在l~100nm之间,故B错误;
C、氯化铁溶液是黄色的液体,氢氧化铁胶体呈红褐色,故C错误;
D、氢氧化铁胶体加热得到氧化铁,氯化铁溶液中铁水解生成氢氧化铁,加热生成氧化铁,故D正确;
故选:D.
点评:本题考查学生胶体的性质以及胶体和溶液的区别,题目难度不大,注意氯化铁溶液是黄色的液体,氢氧化铁胶体是红褐色液体.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案
相关题目
某元素一个原子的质量为ag,一个C-12原子的质量为bg,则该元素的相对原子质量为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
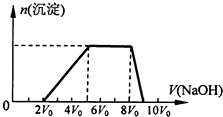 某混合溶液中可能含有的离子如表所示:
某混合溶液中可能含有的离子如表所示:
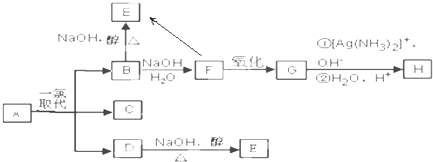
 化合物A相对分子质量为86,碳的质量分数为55.8%,氢为7.0%,其余为氧.A的相关反应如下图所示:
化合物A相对分子质量为86,碳的质量分数为55.8%,氢为7.0%,其余为氧.A的相关反应如下图所示: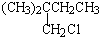 ,B和D分别与强碱的醇溶液共热,都只能得到有机化合物E.以上反应及B的进一步反应如所示.
,B和D分别与强碱的醇溶液共热,都只能得到有机化合物E.以上反应及B的进一步反应如所示.