题目内容
5.总压强为30Mpa时,氮气﹑氢气混合气体(体积比为1:3)通入合成塔,反应达平衡时,压强降为25Mpa则平衡时混合气体中氨气的体积分数为( )| A. | 25% | B. | 20% | C. | 35% | D. | 30% |
分析 根据反应:N2+3H2?2NH3,利用三段式分析,设氮气起始为amol,则氢气起始为bmol,转化的氮气的物质的量为xmol,
N2 +3H2 ?2NH3
起始(mol) a 3a 0
转化(mol) x 3x 2x
平衡(mol) a-x 3a-3x 2x
根据压强之比等于物质的是之比可知$\frac{a-x+3a-3x+2x}{a+3a}$=$\frac{25Mpa}{30Mpa}$,可得x=$\frac{a}{3}$,据此可计算出氨气的体积分数;
解答 解:根据反应:N2+3H2?2NH3,利用三段式分析,设氮气起始为amol,则氢气起始为bmol,转化的氮气的物质的量为xmol,
N2 +3H2 ?2NH3
起始(mol) a 3a 0
转化(mol) x 3x 2x
平衡(mol) a-x 3a-3x 2x
根据压强之比等于物质的是之比可知$\frac{a-x+3a-3x+2x}{a+3a}$=$\frac{25Mpa}{30Mpa}$,可得x=$\frac{a}{3}$,所以氨气的体积分数为$\frac{2×\frac{a}{3}}{4a-2×\frac{a}{3}}$×100%=20%,
故选B.
点评 本题考查化学方程式计算,难度不大,注意充分利用反应前后的压强之比进行计算.

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
20.常温下均不溶于水且比水轻的一组液体是( )
| A. | 溴苯 乙酸 | B. | 硝基苯 氯乙烷 | C. | 甲苯 乙酸乙酯 | D. | 苯 乙醇 |
1.将白醋、食用油、食盐、酒精分别放入水中,不能形成溶液的是( )
| A. | 白醋 | B. | 食用油 | C. | 食盐 | D. | 酒精 |
5.在一密闭容器中有HCHO、H2、和O2混合气体共10g,放入足量Na2O2用电火花引燃,使其完全反应,Na2O2增重4g,则原混合气体中O2的质量分数是( )
| A. | 40% | B. | 33.3% | C. | 60% | D. | 36% |
10.氢气是一种清洁能源.用甲烷制取氢气的两步反应的能量变化如下图所示:
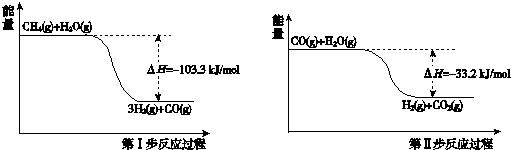
(1)甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式是CH4(g)+2H2O(g)=4H2(g)+CO2(g)△H=-136.5kJ/mol.
(2)第II步为可逆反应.在800℃时,若CO的起始浓度为2.0mol/L,水蒸气的起始浓度为3.0mol/L,达到化学平衡状态后,测得CO2的浓度为1.2mol/L,则此反应的平衡常数为1,随着温度升高该反应的化学平衡常数的变化趋势是变小.
(3)在恒温恒容密闭容器中进行的第II步反应,下列说法中能表示达到平衡状态的是bc(填序号).
a.四种物质的浓度比恰好等于化学方程式中各物质的化学计量数之比
b.单位时间内断开amol H-H键的同时断开2a mol O-H键
c.反应容器中放出的热量不再变化
d.混合气体的密度不再发生变化
e.混合气体的压强不再发生变化
(4)某温度下,第Ⅱ步反应的平衡常数为K=$\frac{1}{9}$.该温度下在甲、乙、丙三个恒容密闭容器中投入H2O(g)和CO(g),其起始浓度如下表所示.下列判断不正确的是CD.
A.反应开始时,丙中的反应速率最快,甲中的反应速率最慢
B.平衡时,甲中和丙中H2O的转化率均是25%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.015mol/L
D.平衡时,乙中H2O的转化率大于25%

(1)甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式是CH4(g)+2H2O(g)=4H2(g)+CO2(g)△H=-136.5kJ/mol.
(2)第II步为可逆反应.在800℃时,若CO的起始浓度为2.0mol/L,水蒸气的起始浓度为3.0mol/L,达到化学平衡状态后,测得CO2的浓度为1.2mol/L,则此反应的平衡常数为1,随着温度升高该反应的化学平衡常数的变化趋势是变小.
(3)在恒温恒容密闭容器中进行的第II步反应,下列说法中能表示达到平衡状态的是bc(填序号).
a.四种物质的浓度比恰好等于化学方程式中各物质的化学计量数之比
b.单位时间内断开amol H-H键的同时断开2a mol O-H键
c.反应容器中放出的热量不再变化
d.混合气体的密度不再发生变化
e.混合气体的压强不再发生变化
(4)某温度下,第Ⅱ步反应的平衡常数为K=$\frac{1}{9}$.该温度下在甲、乙、丙三个恒容密闭容器中投入H2O(g)和CO(g),其起始浓度如下表所示.下列判断不正确的是CD.
| 起始浓度 | 甲 | 乙 | 丙 |
| c(H2O)/mol/L | 0.010 | 0.020 | 0.020 |
| c(CO)/mol/L | 0.010 | 0.010 | 0.020 |
B.平衡时,甲中和丙中H2O的转化率均是25%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.015mol/L
D.平衡时,乙中H2O的转化率大于25%
15.下列离子方程式正确的是( )
| A. | 亚硫酸氢铵溶液中滴加少量NaOH溶液:NH4++OH-═NH3.H2O | |
| B. | 酸性KI淀粉溶液久置后变蓝4I-+O2+2H2O═2I2+4OH- | |
| C. | 铜溶于稀硝酸中:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O | |
| D. | NaHCO3溶液中加足量Ba(OH)2溶液:HCO3-+Ba2++OH-═BaCO3↓+H2O |
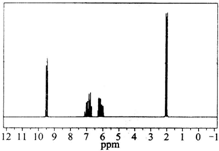 质谱图表明某有机物的相对分子质量为70,红外光谱表征到C═C和C═O的存在,1H核磁共振谱如图(峰面积之比依次为1:1:1:3):
质谱图表明某有机物的相对分子质量为70,红外光谱表征到C═C和C═O的存在,1H核磁共振谱如图(峰面积之比依次为1:1:1:3):