题目内容
【选修2化学与技术】
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.其生产工艺如下:

已知:①2KOH+Cl2=KCl+KClO+H2O(条件:温度较低)
②6KOH+3Cl2=5KCl+KClO3+3H2O(条件:温度较高)
回答下列问题:
(1)该生产工艺应在 (填“温度较高”或“温度较低”)的情况下进行;
(2)在溶液I中加入KOH固体的目的是 (填编号).
A.与溶液I中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供碱性的环境
D.使KClO3转化为 KClO
(3)从溶液II中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为 .
(4)配制KOH溶液时,是在每100mL水中溶解61.6g KOH固体(该溶液的密度为1.47g/mL),它的物质的量浓度为 ;
(5)如何判断K2FeO4晶体已经洗涤干净 .
(6)高铁酸钾(K2FeO4)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,配平该反应的离子方程式: FeO42-+ H2O= Fe(OH)3(胶体)+ O2↑+ OH-.
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.其生产工艺如下:

已知:①2KOH+Cl2=KCl+KClO+H2O(条件:温度较低)
②6KOH+3Cl2=5KCl+KClO3+3H2O(条件:温度较高)
回答下列问题:
(1)该生产工艺应在
(2)在溶液I中加入KOH固体的目的是
A.与溶液I中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供碱性的环境
D.使KClO3转化为 KClO
(3)从溶液II中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为
(4)配制KOH溶液时,是在每100mL水中溶解61.6g KOH固体(该溶液的密度为1.47g/mL),它的物质的量浓度为
(5)如何判断K2FeO4晶体已经洗涤干净
(6)高铁酸钾(K2FeO4)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,配平该反应的离子方程式:
考点:制备实验方案的设计,物质的分离、提纯的基本方法选择与应用
专题:实验设计题
分析:(1)由工艺流程及③可知,利用Fe(NO3)3与KClO制备K2FeO4,由信息②可知温度较高KOH与Cl2 反应生成的是KClO3;
(2)根据生产工艺流程图,第①步氯气过量,反应液I中有过量的Cl2反应,生成更多的KClO,第③步需要碱性条件,在温度较高时KOH 与Cl2 反应生成的是KClO3,氧化还原反应中化合价有升有降;
(3)根据题目信息、氧化还原反应中化合价发生变化确定产物以及电子得失守恒和质量守恒来配平;
(4)依据n=
计算溶质物质的量,结合溶液密度和溶液质量计算溶液体积,结合c=
得到;
(5)检验最后一次的洗涤中无Cl-即可;
(6)根据氧化还原反应电子得失守恒配平.
(2)根据生产工艺流程图,第①步氯气过量,反应液I中有过量的Cl2反应,生成更多的KClO,第③步需要碱性条件,在温度较高时KOH 与Cl2 反应生成的是KClO3,氧化还原反应中化合价有升有降;
(3)根据题目信息、氧化还原反应中化合价发生变化确定产物以及电子得失守恒和质量守恒来配平;
(4)依据n=
| m |
| M |
| n |
| V |
(5)检验最后一次的洗涤中无Cl-即可;
(6)根据氧化还原反应电子得失守恒配平.
解答:
解:(1)由工艺流程及③可知,利用Fe(NO3)3与KClO制备K2FeO4,由信息②可知温度较高KOH与Cl2 反应生成的是KClO3.由信息①可知,在低温下KOH与Cl2 反应生成的是KClO.故选择低温较低,故答案为:温度较低;
(2)由工艺流程可知,反应溶液I中有过量的Cl2反应,加KOH固体的目的是与过量的Cl2继续反应,生成更多的KClO为下一步反应提供反应物;
A、根据生产工艺流程图,第①步氯气过量,加入KOH固体后会继续反应生成KClO,故A正确;
B、因温度较高时KOH 与Cl2 反应生成的是KClO3,而不是KClO,故B错误;
C、第③步需要碱性条件,所以碱要过量,故C正确;
D、KClO3转化为 KClO,化合价只降不升,故D错误;
故答案为:AC;
(3)由题目信息和氧化还原反应中化合价发生变化,可知反应物为Fe3+、ClO-,生成物为FeO42-、Cl-,根据电子得失守恒和质量守恒来配平可得2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O,
故答案为:2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O;
(4)配制KOH溶液时,是在每100mL水中溶解61.6g KOH固体(该溶液的密度为1.47g/mL),溶质物质的量=
=1.1mol,溶液体积V=
=0.11L,它的物质的量浓度=
=10mol/L,故答案为:10mol/L;
(5)因只要检验最后一次的洗涤中无Cl-,即可证明K2FeO4晶体已经洗涤干净,方法为用试管取少量最后一次的洗涤液,加入硝酸银溶液,无白色沉淀则已被洗净,
故答案为:用试管取少量最后一次的洗涤液,加入硝酸银溶液,无白色沉淀则已被洗净;
(6)铁元素化合价+6价变化为+3价,氧元素化合价从0价变化为-2价,由电子守恒配平得到:4FeO42-+10H2O═4Fe(OH)3(胶体)+3O2↑+8OH-,
故答案为:4;10;4;3;8.
(2)由工艺流程可知,反应溶液I中有过量的Cl2反应,加KOH固体的目的是与过量的Cl2继续反应,生成更多的KClO为下一步反应提供反应物;
A、根据生产工艺流程图,第①步氯气过量,加入KOH固体后会继续反应生成KClO,故A正确;
B、因温度较高时KOH 与Cl2 反应生成的是KClO3,而不是KClO,故B错误;
C、第③步需要碱性条件,所以碱要过量,故C正确;
D、KClO3转化为 KClO,化合价只降不升,故D错误;
故答案为:AC;
(3)由题目信息和氧化还原反应中化合价发生变化,可知反应物为Fe3+、ClO-,生成物为FeO42-、Cl-,根据电子得失守恒和质量守恒来配平可得2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O,
故答案为:2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O;
(4)配制KOH溶液时,是在每100mL水中溶解61.6g KOH固体(该溶液的密度为1.47g/mL),溶质物质的量=
| 61.6g |
| 56g/mol |
| 100g+61.6g |
| 1.47g/ml×1000ml/L |
| 1.1mol |
| 0.11L |
(5)因只要检验最后一次的洗涤中无Cl-,即可证明K2FeO4晶体已经洗涤干净,方法为用试管取少量最后一次的洗涤液,加入硝酸银溶液,无白色沉淀则已被洗净,
故答案为:用试管取少量最后一次的洗涤液,加入硝酸银溶液,无白色沉淀则已被洗净;
(6)铁元素化合价+6价变化为+3价,氧元素化合价从0价变化为-2价,由电子守恒配平得到:4FeO42-+10H2O═4Fe(OH)3(胶体)+3O2↑+8OH-,
故答案为:4;10;4;3;8.
点评:本题结合高铁酸钾(K2FeO4)的制备主要考查了氧化还原反应的知识、离子的检验等,培养了学生运用知识的能力,题目难度中等.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
下列反应中,在原理上可以设计成原电池的是( )
| A、Ba(OH)2?8H2O与NH4Cl的反应 |
| B、氢氧化钠与浓硫酸的反应 |
| C、甲烷与氧气的反应 |
| D、石灰石的分解反应 |
下列对X+2Y═X2++2Y-的叙述中正确的是( )
| A、Y被还原,X2+是氧化产物 |
| B、Y被还原,X发生还原反应 |
| C、X是还原剂,Y被氧化 |
| D、X被氧化,X显氧化性 |
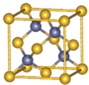 砷化镓为第三代半导体材料,晶胞结构如图所示,
砷化镓为第三代半导体材料,晶胞结构如图所示, 实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏(如图所示),得到含有乙醇、乙酸和水的乙酸乙酯粗产品.请回答下列问题:
实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏(如图所示),得到含有乙醇、乙酸和水的乙酸乙酯粗产品.请回答下列问题: 向139mL密度为1.05g/cm3的CaCl2和HCl混合溶液中滴加Na2CO3溶液,测得生成的沉淀质量(y轴)与加入Na2CO3溶液的体积(x轴)的关系如图,已知原溶液中含CaCl2为7.6%,恰好完全反应时,加入Na2CO3溶液的总质量为191.9g(设此时溶液密度为1.02g/cm3)求:
向139mL密度为1.05g/cm3的CaCl2和HCl混合溶液中滴加Na2CO3溶液,测得生成的沉淀质量(y轴)与加入Na2CO3溶液的体积(x轴)的关系如图,已知原溶液中含CaCl2为7.6%,恰好完全反应时,加入Na2CO3溶液的总质量为191.9g(设此时溶液密度为1.02g/cm3)求: 乙酰水杨酸俗称阿司匹林(
乙酰水杨酸俗称阿司匹林( ),是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128℃~135℃.实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,其制备原理为:
),是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128℃~135℃.实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,其制备原理为: +(CH3CO)2O
+(CH3CO)2O +CH3COOH
+CH3COOH 已知A、B、C、D之间存在如图转化关系,试回答下列问题:
已知A、B、C、D之间存在如图转化关系,试回答下列问题: