题目内容
14.设NA为阿伏加德罗常数的值,下列说法正确的是( )| A. | 64gCaC2中含有的共价键数目为3NA | |
| B. | 20gD2O与20gH218O含有的中子数均为11NA | |
| C. | 4.6gNO2在标准状况下,含有的分子数为0.1 NA | |
| D. | 50ml 12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA |
分析 A、求出碳化钙的物质的量,然后根据碳化钙中含3条共价键来分析;
B、D2O与H218O的摩尔质量均相同,且均含10个中子;
C、NO2中存在平衡:2NO2?N2O4;
D、二氧化锰只能与浓盐酸反应,和稀盐酸不反应.
解答 解:A、64g碳化钙的物质的量为1mol,而碳化钙中含3条共价键,故1mol碳化钙中含3NA条共价键,故A正确;
B、D2O与H218O的摩尔质量均相同,均为20g/mol,故20gD2O与20gH218O的物质的量均为1mol,且两者均含10个中子,故含有的中子的个数均为10NA个,故B错误;
C、NO2中存在平衡:2NO2?N2O4,导致分子个数减少,故含有的分子个数小于0.1NA个,故C错误;
D、二氧化锰只能与浓盐酸反应,和稀盐酸不反应,故浓盐酸不能反应完全,则转移的电子数小于0.3NA个,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.在一定温度下,相一个容积固定的密闭容器中充入2molSO2和1molO2,发生反应2SO2(g)+O2(g)?2SO3(g),反应达到平衡时,测得SO3的浓度为c mol•L-1,若起始时按下列比例配料,则平衡时SO3仍为cmol•L-1的是( )
| A. | 1molSO2、0.5molO2、1molSO3 | B. | 4molSO2、2molO2 | ||
| C. | 4molSO3 | D. | 1molSO2、1molO2、1molSO3 |
2.实验是化学研究的基础,如图装置或操作正确的是( )
| A. | 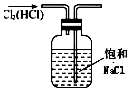 用图所示装置可得到纯净的Cl2 | |
| B. | 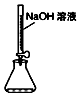 用图量取15.00mL的NaOH溶液 | |
| C. | 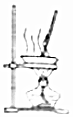 用图所示装置蒸发FeCl3溶液制备无水FeCl2 | |
| D. |  关闭分液漏斗的活塞,从b处加水,以检查装置的气密性 |
9.下列离子方程式书写正确的是( )
| A. | AlCl3溶液与过量的氨水反应:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| B. | 过量的澄清石灰水与碳酸氢钠溶液反应:2HCO3-+2OH-+Ca2+═CaCO3↓+CO32-+2H2O | |
| C. | 硫酸与Ba(OH)2溶液反应:H++OH-=H2O | |
| D. | FeCl3溶液与Fe反应:Fe3++Fe=2Fe2+ |
19.化学与社会、生活、技术和环境密切相关.下列有关说法中不正确的是( )
| A. | 有机溶剂(如乙醚、乙醇、苯、丙酮等)沸点低,极易被引燃,加热时最好用水浴加热 | |
| B. | 石油裂解、海水制镁、纤维素制火棉都包含化学变化 | |
| C. | 大分子化合物油脂在人体内水解为氨基酸和甘油等小分子才能被吸收 | |
| D. | 苹果放在空气中久置变黄和纸张久置变黄原理不同 |
6.相同温度下等物质的量浓度的下列溶液中,c(NH4+)最大的是( )
| A. | CH3COONH4 | B. | NH3•H2O | C. | NH4Cl | D. | NH4HSO4 |
3.下列说法正确的是( )
| A. | 常温常压下,16g O3所含的氧原子数目为NA | |
| B. | 标准状况下,O2的体积取决于O2分子间的距离 | |
| C. | 摩尔是用来衡量微观粒子多少的一种物理量 | |
| D. | 若气体摩尔体积为22.4 L/mol,则所处条件为标准状况 |
4.醇类在我们的日常生话中扮演着重要的角色,下列对于醇类的认识正确的是( )
| A. | 乙二醇和丙三醇互为同系物 | |
| B. | 醇都可以发生消去反应 | |
| C. | 醇在Cu催化作用下都可以催化氧化 | |
| D. | 饱和一元脂肪醇的化学式可用通式CnH2n+2O表示 |