题目内容
12.有些化学仪器加热时需要放在石棉网上,但也有一些仪器可以直接在酒精灯上加热,下列各组仪器中可以用酒精灯直接加热的一组是( )| A. | 坩埚、烧杯 | B. | 试管、燃烧匙 | C. | 蒸发皿、平底烧瓶 | D. | 蒸发皿、圆底烧瓶 |
分析 实验室中可直接加热的仪器有:蒸发皿、试管、坩埚;垫石棉网可加热的有:烧杯、烧瓶、锥形瓶等,不能加热的有集气瓶、广口瓶、细口瓶等,据此进行判断.
解答 解:A.烧杯需要垫石棉网加热,故A错误;
B.试管、燃烧匙能够直接加热,故B正确;
C.平底烧瓶需要垫石棉网加热,故C错误;
D.圆底烧瓶需要垫石棉网加热,故D错误.
故选B.
点评 本题考查直接加热的仪器及使用方法,题目难度不大,注意实验室中一些仪器可以直接加热,有些需垫石棉网,有些根本就不能被加热;试管能直接加热;烧杯、烧瓶、锥形瓶不能直接加热,需垫石棉网;量筒、集气瓶不能加热.

练习册系列答案
相关题目
13.下列实验不能达到预期目的是( )
| A. | 检验C2H5Cl中的氯元素:将C2H5Cl和NaOH溶液混合加热煮沸后,加过量的HNO3酸化,再加AgNO3溶液 | |
| B. | 混有乙酸、乙醇杂质的乙酸乙酯用饱和Na2CO3溶液进行除杂提纯 | |
| C. | 用碘酒验证汽油是否为裂化汽油 | |
| D. | 用溴水(分液)的方法除去己烷中的己烯 |
3.类推法是科学学习的重要方法之一.在学习了卤族元素的各种性质后,如下表所示,表格提供的是氧族元素的部分性质.请结合元素周期律完成下列问题:
(1)硒的熔点范围可能是113~450℃.
(2)碲的化合价可能有-2,+4,+6.
(3)硫、硒、碲的氢化物水溶液的酸性由强至弱的顺序是H2Te>H2Se>H2S(填化学式).
(4)氢硒酸有较强的还原性(填“氧化性”或“还原性”).因此放在空气中长期保存易变质,其可能发生的化学方程式为2H2Se+O2=2H2O+2Se↓.
(5)工业上Al2Te3可用来制备H2Te,完成下列化学方程式:Al2Te3+6H2O----Al(OH)3↓+H2Te↑
| 元素 | 8O | 16S | 34Se | 52Te |
| 单质熔点(℃) | -218.4 | 113 | 450 | |
| 单质沸点(℃) | -183 | 444.6 | 685 | 1390 |
| 主要化合价 | -2 | -2,+4,+6 | -2,+4,+6 | |
| 原子半径 | 逐渐增大 | |||
| 单质与H2 反应情况 | 点燃时 易化合 | 加热化合 | 加热难 化合 | 不能直 接化合 |
(2)碲的化合价可能有-2,+4,+6.
(3)硫、硒、碲的氢化物水溶液的酸性由强至弱的顺序是H2Te>H2Se>H2S(填化学式).
(4)氢硒酸有较强的还原性(填“氧化性”或“还原性”).因此放在空气中长期保存易变质,其可能发生的化学方程式为2H2Se+O2=2H2O+2Se↓.
(5)工业上Al2Te3可用来制备H2Te,完成下列化学方程式:Al2Te3+6H2O----Al(OH)3↓+H2Te↑
20.一块金属钠置于空气中,最终得到的产物是( )
| A. | Na2O | B. | NaOH | C. | Na2O2 | D. | Na2CO3 |
7.相同温度下,根据三种酸的电离常数,下列判断正确的是( )
| 酸 | HX | HY | HZ |
| 电离常数K | 9×10-7 | 9×10-6 | 10-2 |
| A. | 三种酸的强弱关系:HX>HY>HZ | |
| B. | 反应HZ+Y-═HY+Z-能够发生 | |
| C. | 相同温度下,0.1 mol•L-1的HX、HY、HZ溶液,HX与锌反应一定最快 | |
| D. | 相同温度下,1 mol•L-1 HX溶液的电离常数大于0.1 mol•L-1 HX |
17.如图有关实验操作正确的是( )
| A. |  加热液体 | B. |  称取10.05g氢氧化钠 | ||
| C. | 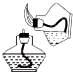 点燃酒精灯 | D. |  量取8.5mL液体 |
2.已知硫酸亚铁溶液中加入过氧化钠时发生反应:4Fe2++4Na2O2+6H2O═4Fe(OH)3↓+O2↑+8Na+,则下列说法正确的是( )
| A. | 该反应中Na2O2既是氧化剂又是还原剂,O2是还原产物 | |
| B. | 若Fe2+失去4mol电子,生成氧气的体积约为22.4L | |
| C. | 4 mol Na2O2在反应中共得到6NA个电子 | |
| D. | 反应过程中可以看到白色沉淀先转化为灰绿色后转化为红褐色 |
 某同学欲配制4mol•L-l的硫酸,但实验室只有三种不同浓度的硫酸:①280ml.1mol•L-l硫酸;②220mL 25%硫酸(p=l.18g.mL-l);③足量的18mol•L-l的浓硫酸.
某同学欲配制4mol•L-l的硫酸,但实验室只有三种不同浓度的硫酸:①280ml.1mol•L-l硫酸;②220mL 25%硫酸(p=l.18g.mL-l);③足量的18mol•L-l的浓硫酸.