题目内容
12.不能用胶体的知识解释的现象是( )| A. | 清晨的阳光穿过茂密的林木枝叶所产生的美丽景象(美丽的光线) | |
| B. | 尿毒症患者使用血液透析治疗 | |
| C. | 明矾净水 | |
| D. | 向FeCl3溶液中加入NaOH溶液,会出现红褐色 |
分析 A.气溶胶具有丁达尔现象;
B.胶体不能通过半透膜,可以通过此性质来精制胶体,分离胶体;
C.明矾净水原理是电离出的铝离子水解生成氢氧化铝胶体具有吸附性;
D.红褐色沉淀是生成的氢氧化铁,不是胶体.
解答 解:A.清晨的阳光穿过茂密的林木枝叶所产生的美丽景象,是胶体的丁达尔现象,与胶体有关,故A不符合;
B.尿毒症主要是血红蛋白随尿液排出,所以血液透析就是将血液通过半透膜,防止血红蛋白流失,故B不符合;
C.明矾净水原理是硫酸铝钾溶液中含有铝离子,铝离子水解Al3++3H2O?Al(OH)3(胶体)+3H+,生成氢氧化铝胶体和氢离子,氢氧化铝胶体具有吸附性净水,和胶体有关,故C不符合;
D.在FeCl3溶液中滴加NaOH溶液出现红褐色沉淀,发生的是复分解反应,与胶体无关,故D错误.
故选D.
点评 本题考查了胶体性质的应用,主要考查胶体的聚沉、胶体的分散质微粒直径,丁达尔现象,熟练掌握胶体性质是解题关键,题目难度不大.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案
相关题目
2.工业上利用电镀污泥 (主要含有Fe2O3、CuO、Cr2O3及部分难溶杂质) 回收铜和铬等金属,回收流程如图1:

已知部分物质沉淀的pH及CaSO4的溶解度曲线如图2:
(1)在浸出过程中除了生成Fe2(SO4)3、Cr2(SO4)3外,主要还有CuSO4.
(2)在除铁操作中,需要除去Fe3+和CaSO4,请完成相关操作:
①加入石灰乳调节pH到约3.2~4.3,检验Fe3+已经除尽的操作是取适量滤液,加KSCN溶液,若不变红,则说明Fe3+已除;
②将浊液加热到80℃,趁热过滤.
(3)写出还原步骤中加入NaHSO3生成Cu2O固体反应的离子方程式:,此步骤中加入NaHSO3得到Cu2O的产率为95%,若NaHSO3过量,除了浪费试剂外,还会出现的问题是产生SO2污染环境.
(4)当离子浓度小于或等于1×10-5mol•L-1时可认为沉淀完全,若要使Cr3+完全沉淀则要保持 c(OH-)≥4.0×10-9 mol•L-1.[已知:Ksp[Cr(OH)3]=6.3×10-31,$\root{3}{63}$≈4.0].

已知部分物质沉淀的pH及CaSO4的溶解度曲线如图2:
| Fe3+ | Cu2+ | Cr3+ | |
| 开始沉淀pH | 2.1 | 4.7 | 4.3 |
| 完全沉淀pH | 3.2 | 6.7 | a |
(2)在除铁操作中,需要除去Fe3+和CaSO4,请完成相关操作:
①加入石灰乳调节pH到约3.2~4.3,检验Fe3+已经除尽的操作是取适量滤液,加KSCN溶液,若不变红,则说明Fe3+已除;
②将浊液加热到80℃,趁热过滤.
(3)写出还原步骤中加入NaHSO3生成Cu2O固体反应的离子方程式:,此步骤中加入NaHSO3得到Cu2O的产率为95%,若NaHSO3过量,除了浪费试剂外,还会出现的问题是产生SO2污染环境.
(4)当离子浓度小于或等于1×10-5mol•L-1时可认为沉淀完全,若要使Cr3+完全沉淀则要保持 c(OH-)≥4.0×10-9 mol•L-1.[已知:Ksp[Cr(OH)3]=6.3×10-31,$\root{3}{63}$≈4.0].
3.下列反应能用H++OH-═H2O 表示的是( )
| A. | NaOH 溶液和CO2 的反应 | B. | Ba(OH)2 溶液和稀H2SO4 的反应 | ||
| C. | NaHSO4溶液和KOH 反应 | D. | 石灰乳和稀H2SO4 的反应 |
20.下列仪器及其名称不正确的是( )
| A. |  蒸馏烧瓶 | B. |  分液漏斗 | C. |  蒸发皿 | D. |  溶量瓶 |
17.若在加入铝粉能放出H2的溶液中,分别加入下列各组离子,可能共存的是( )
| A. | Mg2+、Cl-、Na+、NO3- | B. | K+、Na+、NO3-、HCO3- | ||
| C. | Na+、Ba2+、Cl-、NO3- | D. | Fe3+、Na+、AlO2-、SO42- |
1.动手实践:为了更好的掌握周期表的应用,某同学在做氯、溴、碘性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象
请你帮助该同学整理并完成实验报告.
(1)实验目的:研究同主族元素性质递变规律.
(2)实验用品:试剂:氯水,溴水,NaBr溶液,KI溶液,CCl4溶液仪器:①试管,②胶头滴管.
(3)此实验的结论为氧化性的强弱顺序为:Cl2>Br2>I2.
(4)氯、溴、碘最高价氧化物对应的水化物酸性强弱(用分子式表示):HClO4>HBrO4>HIO4.
(5)氟、氯、溴、碘气态氢化物稳定性大小顺序(用分子式表示):HF>HCl>HBr>HI.
(6)该同学又做了另外一个实验,向新制得的Na2S溶液中滴加新制的氯水.该实验现象为生成淡黄色沉淀.此反应的离子方程式Cl2+S2-=S↓+2Cl-.此实验的结论为氧化性Cl2>S.
| 实验步骤 | 实验现象 |
| ①将少量的氯水滴入到适量NaBr溶液中,再滴入少量的CCl4溶液并用力振荡 | A.溶液分为上下两层,上层为无色,下层为橙红色 |
| ②将少量的溴水滴入到适量KI溶液中,再滴入少量的CCl4溶液并用力振荡 | B.溶液分为上下两层,上层为无色,下层为紫红色 |
(1)实验目的:研究同主族元素性质递变规律.
(2)实验用品:试剂:氯水,溴水,NaBr溶液,KI溶液,CCl4溶液仪器:①试管,②胶头滴管.
(3)此实验的结论为氧化性的强弱顺序为:Cl2>Br2>I2.
(4)氯、溴、碘最高价氧化物对应的水化物酸性强弱(用分子式表示):HClO4>HBrO4>HIO4.
(5)氟、氯、溴、碘气态氢化物稳定性大小顺序(用分子式表示):HF>HCl>HBr>HI.
(6)该同学又做了另外一个实验,向新制得的Na2S溶液中滴加新制的氯水.该实验现象为生成淡黄色沉淀.此反应的离子方程式Cl2+S2-=S↓+2Cl-.此实验的结论为氧化性Cl2>S.
18.某温度,在1L恒容密闭容器中,加入10molCO、7molH2S,发生如下反应:CO(g)+H2S(g)?COS(g)+H2(g),达平衡时CO物质的量为8mol,下列说法正确的是( )
| A. | 该温度下,化学平衡常数K=0.1 | |
| B. | H2S的平衡转化率为20% | |
| C. | 增大CO浓度,平衡正向移动,可以提高CO的转化率 | |
| D. | 升高温度,H2S浓度增加,表明该反应正方向是吸热反应 |
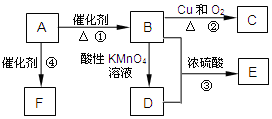 有机物A是来自石油的重要有机化工原料,此物质可以用来衡量一个国家石油化工发展水平.C在一定条件下也会生成D,D能使石蕊溶液变红;E是具有果香味的有机物,F是一种高分子化合物,可制成多种包装材料.
有机物A是来自石油的重要有机化工原料,此物质可以用来衡量一个国家石油化工发展水平.C在一定条件下也会生成D,D能使石蕊溶液变红;E是具有果香味的有机物,F是一种高分子化合物,可制成多种包装材料.