题目内容
下列离子方程式正确的是( )
| A、硫酸铝溶液中加过量氨水:Al3++4OH-=AlO2-+2H2O |
| B、向硅酸钠溶液中通入过量的CO2:SiO32-+2CO2+2H2O=H2SiO3↓+2HCO3- |
| C、过量铁粉与一定量稀硝酸反应:Fe+4H++NO3-=Fe3++NO↑+2H2O |
| D、向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至刚好沉淀完全:Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3?H2O+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.弱电解质写化学式,氢氧化铝不溶于弱碱;
B.二者反应生成硅酸和碳酸氢钠;
C.二者反应生成亚铁离子和NO;
D.要使二者刚好沉淀完全,二者应该以1:1混合,反应后生成硫酸钡、一水合氨和水.
B.二者反应生成硅酸和碳酸氢钠;
C.二者反应生成亚铁离子和NO;
D.要使二者刚好沉淀完全,二者应该以1:1混合,反应后生成硫酸钡、一水合氨和水.
解答:
解:A.弱电解质写化学式,氢氧化铝不溶于弱碱,离子方程式为Al3++3NH3.H2O=Al(OH)3↓+3NH4+,故A错误;
B.二者反应生成硅酸和碳酸氢钠,离子方程式为SiO32-+2CO2+2H2O=H2SiO3↓+2HCO3-,故B正确;
C.二者反应生成亚铁离子和NO,离子方程式为3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O,故C错误;
D.要使二者刚好沉淀完全,二者应该以1:1混合,反应后生成硫酸钡、一水合氨和水,离子方程式为Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3?H2O+H2O,故D正确;
故选BD.
B.二者反应生成硅酸和碳酸氢钠,离子方程式为SiO32-+2CO2+2H2O=H2SiO3↓+2HCO3-,故B正确;
C.二者反应生成亚铁离子和NO,离子方程式为3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O,故C错误;
D.要使二者刚好沉淀完全,二者应该以1:1混合,反应后生成硫酸钡、一水合氨和水,离子方程式为Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3?H2O+H2O,故D正确;
故选BD.
点评:本题考查离子方程式正误判断,为考查热点,明确物质的性质及离子方程式书写规则是解本题关键,注意:A中氢氧化铝不溶于弱碱,注意BD中反应物的量,反应物的量影响生成物,这些都是易错点.

练习册系列答案
相关题目
下列各组混合物中,不能通过分液进行分离的是( )
| A、溴乙烷和水 | B、甲苯和水 |
| C、乙醛和乙醇 | D、乙醛和水 |
下列关于16O和18O的说法正确的是( )
| A、16O和18O是同一种核素 |
| B、16O和18O核外电子数与中子数均不同 |
| C、通过化学变化可以实现16O与18O间的相互转化 |
| D、1mol16O2和1mol18O2的质量不同 |
经研究发现有白蚁信息素有: (2,4-二甲基-1-庚烯),
(2,4-二甲基-1-庚烯), (3,7-二甲基-1-辛烯),家蚕的性信息素为:CH3(CH2)8CH=CH-CH=CH(CH2)8CH3.下列说法正确的是( )
(3,7-二甲基-1-辛烯),家蚕的性信息素为:CH3(CH2)8CH=CH-CH=CH(CH2)8CH3.下列说法正确的是( )
 (2,4-二甲基-1-庚烯),
(2,4-二甲基-1-庚烯), (3,7-二甲基-1-辛烯),家蚕的性信息素为:CH3(CH2)8CH=CH-CH=CH(CH2)8CH3.下列说法正确的是( )
(3,7-二甲基-1-辛烯),家蚕的性信息素为:CH3(CH2)8CH=CH-CH=CH(CH2)8CH3.下列说法正确的是( )| A、以上三种信息素互为同系物 |
| B、以上三种信息素均能使溴的四氯化碳溶液褪色 |
| C、2,4-二甲基-1-庚烯与3,7-二甲基-1-辛烯互为同分异构体 |
| D、家蚕信息素与1molBr2加成产物只有一种 |
T℃时,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图(Ⅰ).若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ),则下列结论正确的是( )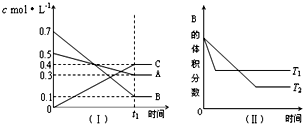

| A、在(t1+10)min时,保持其他条件不变,增大压强,平衡向逆反应方向移动 |
| B、(t1+10)min时,保持容器体积不变,通入稀有气体,平衡向逆反应方向移动 |
| C、其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率减小 |
| D、T℃时,在相同容器中,若由0.4mo1?L-1 A、0.4mo1?L-1 B和0.2mo1?L-1 C反应,达到平衡后,C的浓度为0.4mo1?L-1 |
下列叙述正确的是( )
| A、两种元素构成的共价化合物分子中的化学键不一定是极性键 |
| B、含有非极性键的化合物不一定是共价化合物 |
| C、只要是离子化合物,其熔点就一定比共价化合物的熔点高 |
| D、金属晶体的熔点都比原子晶体低 |