题目内容
5.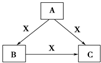 A、B、C、X均为中学化学常见物质,一定条件下有如图所示转化关系(其他产物已略去),下列说法错误的是( )
A、B、C、X均为中学化学常见物质,一定条件下有如图所示转化关系(其他产物已略去),下列说法错误的是( )| A. | 若X为Cl2,则C可为FeCl3 | |
| B. | 若X为KOH溶液,则A可为AlCl3 | |
| C. | 若X为O2,则A可为碳 | |
| D. | 若A、B、C均为焰色反应呈黄色的化合物,则X可为CO2 |
分析 A.若X为Cl2,则B中应是铁离子;
B、若X为KOH溶液,则A可为AlCl3,B为氢氧化铝,C为偏铝酸钾;
C、若X为O2,则A可为碳,则B为一氧化碳,C为二氧化碳;
D、若A、B、C均为焰色反应呈黄色的化合物,A为氢氧化钠,B为碳酸钠,C为碳酸氢钠,则X可为CO2;
解答 解:A.若X为Cl2,则B中应是铁离子,不符合A→B,故A错误;
B、若X为KOH溶液,则A可为AlCl3,B为氢氧化铝,C为偏铝酸钾,符合A→B→C,同时符合:A→C,故B正确;
C、若X为O2,则A可为碳,则B为一氧化碳,C为二氧化碳,符合A→B→C,同时符合:A→C,故C正确;
D、若A、B、C均为焰色反应呈黄色的化合物,A为氢氧化钠,B为碳酸钠,C为碳酸氢钠,则X可为CO2,符合A→B→C,同时符合:A→C,故D正确;
故选A.
点评 本题考查了元素化合物性质与转化,注意掌握中学常见连续反应,熟练掌握元素化合物的性质是解题关键.

练习册系列答案
相关题目
9.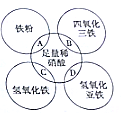 已知稀硝酸是强氧化性酸,还原产物一般为NO,如图两圆相交部分A、B、C、D分别表示两物质间的反应,下列各对应反应的离子方程式书写不正确的是( )
已知稀硝酸是强氧化性酸,还原产物一般为NO,如图两圆相交部分A、B、C、D分别表示两物质间的反应,下列各对应反应的离子方程式书写不正确的是( )
 已知稀硝酸是强氧化性酸,还原产物一般为NO,如图两圆相交部分A、B、C、D分别表示两物质间的反应,下列各对应反应的离子方程式书写不正确的是( )
已知稀硝酸是强氧化性酸,还原产物一般为NO,如图两圆相交部分A、B、C、D分别表示两物质间的反应,下列各对应反应的离子方程式书写不正确的是( )| A. | Fe+4H++NO3-═Fe3++NO↑+2H2O | |
| B. | Fe3O4+8H+═Fe2++2Fe3++4H2O | |
| C. | Fe(OH)3+3H+═Fe3++3H2O | |
| D. | 3Fe(OH)2+10H++NO3-═3Fe3++NO↑+8H2O |
16.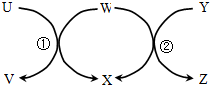 如图中U→Z六种物质在适当条件下能实现图示箭头方向一步转化,且反应①、②均为置换反应,满足条件的物质组是( )
如图中U→Z六种物质在适当条件下能实现图示箭头方向一步转化,且反应①、②均为置换反应,满足条件的物质组是( )
 如图中U→Z六种物质在适当条件下能实现图示箭头方向一步转化,且反应①、②均为置换反应,满足条件的物质组是( )
如图中U→Z六种物质在适当条件下能实现图示箭头方向一步转化,且反应①、②均为置换反应,满足条件的物质组是( )| 序号 | U | W | Y | X |
| ① | Na | H2O | Na2O2 | NaOH |
| ② | Fe | H2O | C | H2 |
| ③ | HBr | Cl2 | CH4 | HCl |
| ④ | CuCl2(aq) | Al | HCl(aq) | AlCl3(aq) |
| A. | ②④ | B. | ②③ | C. | ①②④ | D. | ①②③④ |
13.江苏有着丰富的海水资源,合理利用资源和保护环境是我省可持续发展的重要保证.
(1)海水经过处理后可以得到无水氯化镁,无水氯化镁是工业制取镁的原料.试写出由无水氯化镁制取金属镁的化学反应方程式MgCl2 $\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑.
(2)某化工厂生产过程中会产生含有Cu2+和Pb2+的污水.排放前拟用沉淀法除去这两种离子,根据下列数据,你认为投入Na2S(选填“Na2S”或“NaOH”)效果更好.
(3)火力发电在江苏的能源利用中占较大比重,但是排放出的SO2会造成一系列环境和生态问题.利用海水脱硫是一种有效的方法,其工艺流程如图所示: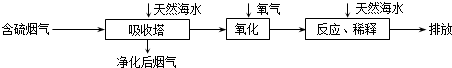
①天然海水的pH≈8海水中主要含有Na+、K+、Ca2+、Mg2+、Cl-、SO42-、Br-、CO32-、HCO3-等离子,试用离子方程式解释天然海水呈弱碱性的原因CO32-+H2O?HCO3-+OH-或 HCO3-+H2O?H2CO3+OH-(任写一个).
②某研究小组为探究提高含硫烟气中SO2的吸收效率的措施,进行了天然海水吸收含硫烟气的模拟实验,实验结果如图所示.

请你根据图示实验结果,就如何提高一定浓度含硫烟气中SO2的吸收效率,提出一条合理化建议:降低含硫烟气温度(或流速).
③天然海水吸收了含硫烟气后会溶有H2SO3、HSO3-等分子或离子,通入氧气氧化的化学原理是2H2SO3+O2=4H++2SO42-或2HSO3-+O2=2H++2SO42-(任写一个化学方程式或离子方程式).氧化后的“海水”需要引入大量的天然海水与之混合后才能排放,该操作的主要目的是中和、稀释经氧气氧化后海水中生成的酸(H+).
(1)海水经过处理后可以得到无水氯化镁,无水氯化镁是工业制取镁的原料.试写出由无水氯化镁制取金属镁的化学反应方程式MgCl2 $\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑.
(2)某化工厂生产过程中会产生含有Cu2+和Pb2+的污水.排放前拟用沉淀法除去这两种离子,根据下列数据,你认为投入Na2S(选填“Na2S”或“NaOH”)效果更好.
| 难溶电解质 | Cu(OH)2 | CuS | Pb(OH)2 | PbS |
| Ksp | 4.8×10-20 | 6.3×10-36 | 1.2×10-15 | 1.0×10-28 |

①天然海水的pH≈8海水中主要含有Na+、K+、Ca2+、Mg2+、Cl-、SO42-、Br-、CO32-、HCO3-等离子,试用离子方程式解释天然海水呈弱碱性的原因CO32-+H2O?HCO3-+OH-或 HCO3-+H2O?H2CO3+OH-(任写一个).
②某研究小组为探究提高含硫烟气中SO2的吸收效率的措施,进行了天然海水吸收含硫烟气的模拟实验,实验结果如图所示.

请你根据图示实验结果,就如何提高一定浓度含硫烟气中SO2的吸收效率,提出一条合理化建议:降低含硫烟气温度(或流速).
③天然海水吸收了含硫烟气后会溶有H2SO3、HSO3-等分子或离子,通入氧气氧化的化学原理是2H2SO3+O2=4H++2SO42-或2HSO3-+O2=2H++2SO42-(任写一个化学方程式或离子方程式).氧化后的“海水”需要引入大量的天然海水与之混合后才能排放,该操作的主要目的是中和、稀释经氧气氧化后海水中生成的酸(H+).
20.化学与生活、社会密切相关.下列说法错误的是( )
| A. | 二氧化硫能使织物褪色,对金属材料也有腐蚀作用 | |
| B. | 大量焚烧田间秸秆会污染空气 | |
| C. | 漂白粉在空气中能稳定存在,可用于漂白纸张 | |
| D. | PM2.5是指大气中直径小于或等于2.5微米(2.5×10-6m)的细小可吸入颗粒物,其分散在空气中可能形成胶体 |
10.下列说法不正确的是( )
| A. | 热的纯碱溶液比冷的纯碱溶液去油污效果好 | |
| B. | 盛放Na2CO3溶液的试剂瓶不能用橡胶塞 | |
| C. | 将AlCl3溶液加热、蒸干、灼烧,可得到固体Al2O3 | |
| D. | 铁在潮湿的环境下生锈与盐类水解无关 |
17.表示下列变化的化学用语不正确的是( )
| A. | 氨水显碱性:NH3•H2O?NH4++OH- | |
| B. | Na2S溶液显碱性:S2-+2H2O?H2S+2OH- | |
| C. | 硫酸氢钠溶液显酸性:NaHSO4═Na++H++SO42- | |
| D. | FeCl3溶液显酸性:Fe3++3H2O?Fe(OH)3+3H+ |
14.下列有关化学用语表示正确的是( )
| A. | HCl的电子式: | B. | ${\;}_{8}^{18}$O2-离子的原子结构示意图: | ||
| C. | CO2分子的结构式:O=C=O | D. | 四氯化碳分子比例模型: |
15.氧元素在周期表中的位置是( )
| A. | 第二期ⅣA族 | B. | 第三期ⅥA族 | C. | 第二期ⅥA族 | D. | 第三期ⅣA族 |