题目内容
12.常温下,将①中溶液滴入②中,预测的现象与实际相符的是( )| 选项 | ①中物质 | ②中物质 | 预测②中的现象 |
| A | 稀盐酸 | 纯碱溶液 | 立即产生气泡 |
| B | 氯化铝溶液 | 浓氢氧化钠溶液 | 立即产生白色沉淀 |
| C | 稀盐酸 | 偏铝酸钠溶液 | 立即产生白色沉淀 |
| D | 稀硫酸 | 酸性高锰酸钾溶液 | 溶液逐渐褪色 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.开始纯碱过量,与盐酸反应生成碳酸氢钠;
B.开始NaOH过量,与氯化铝反应生成偏铝酸钠;
C.开始偏铝酸钠过量,与盐酸反应生成氢氧化铝沉淀;
D.高锰酸钾与稀硫酸不反应.
解答 解:A.开始纯碱过量,与盐酸反应生成碳酸氢钠,则不能立即生成气体,故A错误;
B.开始NaOH过量,与氯化铝反应生成偏铝酸钠,则开始无沉淀生成,故B错误;
C.开始偏铝酸钠过量,与盐酸反应生成氢氧化铝沉淀,则立即产生白色沉淀,故C正确;
D.高锰酸钾与稀硫酸不反应,溶液不能褪色,故D错误;
故选C.
点评 本题考查物质的性质及反应,为高频考点,把握发生的反应及现象为解答的关键,侧重分析与应用能力的考查,注意与量有关的反应,题目难度不大.

练习册系列答案
 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
2.下列化学用语正确的是( )
①羟基的电子式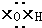 ②乙烯的结构简式:CH2=CH2
②乙烯的结构简式:CH2=CH2
③甲烷的结构式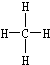 ④乙烯的结构式:C2H4
④乙烯的结构式:C2H4
⑤乙醛的结构简式 CH3COH ⑥硫化氢的电子式 H+[:S:]2-H+.
①羟基的电子式
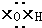 ②乙烯的结构简式:CH2=CH2
②乙烯的结构简式:CH2=CH2③甲烷的结构式
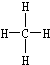 ④乙烯的结构式:C2H4
④乙烯的结构式:C2H4⑤乙醛的结构简式 CH3COH ⑥硫化氢的电子式 H+[:S:]2-H+.
| A. | ①④ | B. | ②④⑥ | C. | ②③ | D. | ②③⑤ |
3.某元素X的核外电子数等于核内中子数,取该元素单质2.8克与氧充分作用,可得到6克化合物XO2.下列说法正确的是( )
| A. | 该元素位于第2周期 | |
| B. | 该元素位于第VI A族 | |
| C. | 该元素的氢化物溶于水显碱性 | |
| D. | 该元素最高价氧化物的水化物是一种弱酸 |
7.下列关于常见有机化合物的说法中正确的是( )
| A. | 乙烷和Cl2在光照条件下反应生成6中氯代产物 | |
| B. | 将苯加入溴水中,振荡后水层接近无色,是因为发生了取代反应 | |
| C. | 乙醇、乙酸、乙酸乙酯都能发生取代反应,乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去 | |
| D. | 糖类、油脂和蛋白质都是人体必须的营养物质,他们的组成元素相同 |
17.下列有关有机物的叙述不正确的是( )
| A. | C4H8O2的酯有4种结构 | |
| B. | 淀粉和纤维素互为同分异构体 | |
| C. | 乙醇和葡萄糖均能发生酯化反应 | |
| D. | 用氢氧化钠溶液可以鉴别地沟油和矿物油 |
4.室温时,下列溶液等体积混合后pH一定小于7的是( )
| A. | pH=3的盐酸和pH=11的氨水 | |
| B. | pH=3的盐酸和pH=11的氢氧化钡溶液 | |
| C. | pH=3的硫酸和pH=11的氨水 | |
| D. | pH=3的醋酸和pH=11的氢氧化钡溶液 |
2.能够大量共存的离子组合是( )
| A. | H+、SO42-、NO3-、Ba2+ | B. | K+、Cl-、CO32-、Na+ | ||
| C. | Cu2+、NO3-、OH-、Na+ | D. | K+、SO42-、HCO3-、H+ |
