题目内容
将4molA气体和2molB气体在2L的容器中混合,并在一定条件下发生如下反应:2A(g)+B(g)?2C(g).若经过2s测得C的浓度为0.6mol/L,现有下列几种说法,其中正确的是( )
①A表示的平均反应速率为0.3mol/L?S
②B表示的平均反应速率为0.6mol/L?S
③2s时物质A的转化率为70%
④2s时物质B的浓度为0.7mol/L.
①A表示的平均反应速率为0.3mol/L?S
②B表示的平均反应速率为0.6mol/L?S
③2s时物质A的转化率为70%
④2s时物质B的浓度为0.7mol/L.
| A、①③ | B、①④ | C、②③ | D、③④ |
考点:化学平衡的计算
专题:化学平衡专题
分析:将 4mol A 气体和 2mol B 气体在 2L 的密闭容器中混合并在一定条件下发生如下反应 2A(g)+B(g)?2C(g),若经 2s(秒)后测得 C 的浓度为0.6mol?L-1?s-1 ,依据化学平衡三段式列式计算
2A(g)+B(g)?2C(g)
起始量(mol) 4 2 0
变化量(mol) 1.2 0.6 1.2
2s末(mol) 2.8 1.4 2L×0.6mol/L=1.2mol
①用物质B表示反应的平均速率=
=0.3mol/L?s;
②用物质B表示反应的平均速率=
=0.15mol/L?s;
③2s末物质A的转化率=
×100%=30%;
④2s末物质B的浓度=
=0.7mol?L-1.
2A(g)+B(g)?2C(g)
起始量(mol) 4 2 0
变化量(mol) 1.2 0.6 1.2
2s末(mol) 2.8 1.4 2L×0.6mol/L=1.2mol
①用物质B表示反应的平均速率=
| ||
| 2 |
②用物质B表示反应的平均速率=
| ||
| 2 |
③2s末物质A的转化率=
| 1.2 |
| 4 |
④2s末物质B的浓度=
| 1.4 |
| 2 |
解答:
解:将 4mol A 气体和 2mol B 气体在 2L 的密闭容器中混合并在一定条件下发生如下反应 2A(g)+B(g)?2C(g),若经 2s(秒)后测得 C 的浓度为0.6mol?L-1?s-1 ,依据化学平衡三段式列式计算
2A(g)+B(g)?2C(g)
起始量(mol) 4 2 0
变化量(mol) 1.2 0.6 1.2
2s末(mol) 2.8 1.4 2L×0.6mol/L=1.2mol
①用物质B表示反应的平均速率=
=0.3mol/L?s;
②用物质B表示反应的平均速率=
=0.15mol/L?s;
③2s末物质A的转化率=
×100%=30%;
④2s末物质B的浓度=
=0.7mol?L-1;
故正确的是①④,
故选B.
2A(g)+B(g)?2C(g)
起始量(mol) 4 2 0
变化量(mol) 1.2 0.6 1.2
2s末(mol) 2.8 1.4 2L×0.6mol/L=1.2mol
①用物质B表示反应的平均速率=
| ||
| 2 |
②用物质B表示反应的平均速率=
| ||
| 2 |
③2s末物质A的转化率=
| 1.2 |
| 4 |
④2s末物质B的浓度=
| 1.4 |
| 2 |
故正确的是①④,
故选B.
点评:本题考查化学平衡三段式计算应用,主要是化学反应速率计算,转化率的计算应用,题目较简单.

练习册系列答案
相关题目
某溶液中含有两种溶质NaCl和H2SO4,它们的物质的量之比为3:1.用石墨做电极电解该混合溶液时,根据电极产物,可明显分为三个阶段,下列叙述不正确的是( )
| A、阴极自始至终只有H2 |
| B、阳极先析出Cl2后析出O2 |
| C、电解最后阶段为电解水 |
| D、溶液pH不断增大,最后为7 |
11.9g金属锡跟100mL12mol?L-1HNO3共热一段时间.完全反应后测定溶液中c(H+)为8mol?L-1,溶液体积仍为100mL.放出的气体在标准状况下体积约为8.96L.由此推断氧化产物可能是(Sn的相对原子质量为119)( )
| A、SnO2?4H2O |
| B、Sn(NO3)4 |
| C、Sn(NO3)2 |
| D、Sn(NO3)2和Sn(NO3)4 |
下列物质能发生加成,加聚和缩聚反应的是( )
| A、C6H5-OH |
B、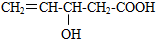 |
| C、CH2=CH-COOH |
| D、HO-CH2-CH=CH-CH2-CH3 |
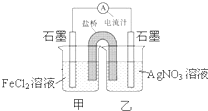 控制适合的条件,将反应Ag+Fe3+?Fe2++Ag+ 设计成如图所示的原电池.下列判断错误的是( )
控制适合的条件,将反应Ag+Fe3+?Fe2++Ag+ 设计成如图所示的原电池.下列判断错误的是( )| A、反应开始时,电子从甲中石墨经导线流向乙中石墨 |
| B、电流计指针为零时,上述反应的正反应速率等于逆反应速率 |
| C、电流计读数为零后,在甲中加入FeCl3固体,甲中石墨电极为负极 |
| D、电流计读数为零后,在甲中加入双氧水,甲中石墨电极反应式是Fe3++e-=Fe2+ |
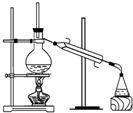
用酒精灯加热下列溶液,蒸干后灼烧,所得固体质量最大的是( )
| A、20 mL 2 mol/L FeCl3溶液 |
| B、40 mL 1 mol/L NaHCO3溶液 |
| C、20 mL 1 mol/L Na2SO3溶液 |
| D、40 mL 2 mol/L NH4HCO3溶液 |


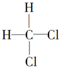 与
与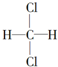 ;④
;④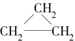 与
与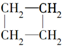
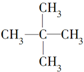 和
和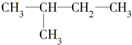 ;⑥
;⑥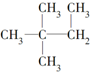 和CH3C(CH3)2CH2CH2CH3.
和CH3C(CH3)2CH2CH2CH3.