题目内容
下列说法错误的是( )
| A、“地沟油”不能食用但可以用来制肥皂 |
| B、利用氢氧化铝的碱性可将其作为治疗某种胃病的内服药 |
| C、食用白糖的主要成分是葡萄糖 |
| D、食用醋是一种常用的调味剂,它的有效成分是乙酸 |
考点:油脂的性质、组成与结构,羧酸简介,葡萄糖的性质和用途,常见的食品添加剂的组成、性质和作用
专题:有机化学基础
分析:A、油脂碱性条件下水解,可生成肥皂;
B、氢氧化铝可以中和胃酸;
C、白糖的主要成分是蔗糖;
D、食醋的主要成分是乙酸,具有酸味.
B、氢氧化铝可以中和胃酸;
C、白糖的主要成分是蔗糖;
D、食醋的主要成分是乙酸,具有酸味.
解答:
解:A、地沟油的主要成分是油脂,油脂碱性条件下水解成为造化反应,可生成肥皂,故A正确;
B、氢氧化铝可以中和胃酸,反应温和,刺激性小,故B正确;
C、白糖的主要成分是蔗糖,故C错误;
D、食醋的主要成分是乙酸,具有酸味,常作调味剂,故D正确;
故选C.
B、氢氧化铝可以中和胃酸,反应温和,刺激性小,故B正确;
C、白糖的主要成分是蔗糖,故C错误;
D、食醋的主要成分是乙酸,具有酸味,常作调味剂,故D正确;
故选C.
点评:本题考查了油脂、糖类、调味剂和抗酸药的主要成分和性质,难度不大,注意生活常识的积累.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目
已知298K时,Mg(OH)2的溶度积常数为KSP=5.6×10-12,取适量的MgCl2溶液,加入一定量的烧碱溶液达到沉淀溶解平衡,测得pH=13.0,则下列说法不正确的是( )
| A、所加烧碱溶液的pH=13.0 |
| B、所得溶液中c(Mg2+)=5.6×10-10mol/L |
| C、所得溶液中c(H+)=1.0×10-13mol/L |
| D、所得溶液中由水电离产生的c(OH-)=1.0×10-13mol/L |
原子序数大于4的主族元素X、Y的离子Xm+、Yn-电子层结构相同,则X、Y的下列叙述正确的是( )
①原子序数X>Y ②X和Y在同一周期 ③Y与X族序数之差是8-(m+n) ④X、Y核电荷数差为(m-n)
①原子序数X>Y ②X和Y在同一周期 ③Y与X族序数之差是8-(m+n) ④X、Y核电荷数差为(m-n)
| A、①③ | B、②④ | C、①② | D、①②③ |
有机化合物A的分子式是C13H20O8(相对分子质量为304),1mol A在酸性条件下水解得到4mol CH3COOH和1mol B.B分子结构中每一个连有羟基的碳原子上还连有两个氢原子.B不能发生的反应是( )
| A、氧化反应 | B、取代反应 |
| C、消去反应 | D、加聚反应 |
分子式C5H12O的有机物,能与钠反应放出H2的有几种?( )
| A、8 | B、4 | C、6 | D、7 |
亮菌甲素适用于治疗急性胆囊炎,其结构简式如图.下列有关叙述正确的是( )
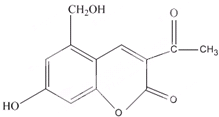

| A、亮菌甲素分子式为C12H11O5 |
| B、1mol亮菌甲素最多能与6mol H2发生加成反应 |
| C、1mol亮菌甲素与NaOH溶液反应,最多消耗3mol NaOH |
| D、亮菌甲素具有弱酸性体现了羟基对苯环的影响 |
下列离子方程式不正确的是( )
| A、向AgCl悬浊液中加入Na2S溶液:2AgCl+S2-═Ag2S+2Cl- |
| B、向NaHCO3溶液中加入NaOH溶液:HCO3-+OH-═CO2↑+H2O |
| C、向Ba(OH)2溶液中加入稀H2SO4:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
| D、向Cu粉中加入过量的浓HNO3:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O |
常温下,下列各组离子在指定的溶液中可能大量共存的是( )
| A、无色透明的溶液中:K+、NH4+、MnO4-、SO42- |
| B、含大量Fe3+的溶液中:Na+、Cu2+、NO3-、I- |
| C、乙醇溶液中:CH3COO-、Al3+、SO42-、Cl- |
| D、由水电离出的c(H+)=1.0×10-11?L-1的溶液中:Fe(OH)3胶体、Ba2+、OH-、Cl- |
烃分子中若含有双键、三键或环,其碳原子所结合的氢原子数则少于碳原子数对应烷烃所含有的氢原子数,亦具有一定的不饱和度(用Ω表示).下表列出几种烃的不饱和度:
据此下列说法不正确的是( )
| 有机物 | 乙烯 | 乙炔 | 环己烷 | 苯 |
| Ω | 1 | 2 | 1 | 4 |
| A、1molΩ=3的不饱和链烃再结合3mol H2,即达到饱和 |
B、 的Ω=7 的Ω=7 |
| C、C4H8的不饱和度与C3H6、C2H4的不饱和度不一定相同 |
| D、CH3CH2CH=CH2与环丁烷的不饱和度相同 |