题目内容
亚氯酸钠(NaClO2)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。它在碱性环境中稳定存在。某同学查阅资料后设计生产NaClO2的主要流程如下。

(1)Ⅰ中发生反应的还原剂是 (填化学式)。
(2)Ⅱ中反应的离子方程式是 。
(3)A的化学式是 ,气体b的化学式是 ,装置Ⅲ中发生反应的化学方程式是 。
(4)ClO2是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备:5NaClO2 + 4HCl = 5NaCl + 4ClO2↑ + 2H2O。
①该反应中氧化剂和还原剂的物质的量之比是 。
②研究表明:若反应开始时盐酸浓度越大,则气体产物中Cl2的含量越大,运用氧化还原反应规律分析其原因是 。
(1)Na2SO3 (2)2ClO2 + H2O2 + 2OH- = 2ClO + O2↑+ 2H2O
+ O2↑+ 2H2O
(3)H2SO4 (1分) H2 (1分)2H2O 2H2↑+ O2↑
2H2↑+ O2↑
(4)1∶4 ClO 的氧化性或Cl-的还原性随溶液的酸性和浓度的增大而增强,因此Cl-被氧化得到Cl2
的氧化性或Cl-的还原性随溶液的酸性和浓度的增大而增强,因此Cl-被氧化得到Cl2
【解析】
试题分析:(1)根据题给流程知,Ⅰ中发生反应为氯酸钠和硫酸钠反应生成二氧化氯和硫酸钠,其中Na2SO3中硫元素的化合价由+4价变成+6价,作还原剂;(2)根据题给流程知,Ⅱ中反应物为ClO2、H2O2和氢氧化钠,产物为NaClO2,ClO2作氧化剂,H2O2中氧元素的化合价由―1价变成0价,离子方程式为2ClO2 + H2O2 + 2OH-= 2ClO2-+ O2↑+ 2H2O;(3)由上述分析知,气体a为氧气,故Ⅲ中阳极反应:2H2O―4e―=4H+ +O2↑,a为O2,阴极:4H2O+4e―=4OH― +2H2↑, b为H2, A的化学式是H2SO4,装置Ⅲ中发生反应的化学方程式是2H2O  2H2 ↑+ O2↑。(4)① 反应5NaClO2 + 4HCl = 5NaCl + 4ClO2↑ + 2H2O中NaClO2氯元素的化合价由+3价分别变为—1价和+4价,NaClO2既是氧化剂又是还原剂,氧化剂和还原剂的物质的量之比是1∶4。② 研究表明:若反应开始时盐酸浓度越大,则气体产物中Cl2的含量越大,运用氧化还原反应规律分析其原因是ClO
2H2 ↑+ O2↑。(4)① 反应5NaClO2 + 4HCl = 5NaCl + 4ClO2↑ + 2H2O中NaClO2氯元素的化合价由+3价分别变为—1价和+4价,NaClO2既是氧化剂又是还原剂,氧化剂和还原剂的物质的量之比是1∶4。② 研究表明:若反应开始时盐酸浓度越大,则气体产物中Cl2的含量越大,运用氧化还原反应规律分析其原因是ClO 的氧化性或Cl-的还原性随溶液的酸性和浓度的增大而增强,因此Cl-被氧化得到Cl2。
的氧化性或Cl-的还原性随溶液的酸性和浓度的增大而增强,因此Cl-被氧化得到Cl2。
考点:考查氧化还原反应,含氯化合物的性质。

某学生用NaHCO3和KHCO3组成的某固体混合物进行实验,测得如下表数据(盐酸的物质的量浓度相等):
实验编号 | ① | ② | ③ |
盐酸体积 | 50mL盐酸 | 50mL盐酸 | 50mL盐酸 |
m(混合物) | 9.2g | 16.56g | 27.6g |
V(CO2)(标准状况) | 2.24L | 3.36L | 3.36L |
分析表中数据,下列说法不正确的是( )
A.由①可以计算出盐酸的物质的量浓度
B.由②、③可知:混合物质量增加,气体体积没有变化,说明盐酸已经反应完全
C.由①、②可知:①中的固体不足而完全反应
D.由①可以计算出混合物的NaHCO3的质量分数
根据表中信息判断,下列选项不正确的是
序号 | 反应物 | 产物 |
① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4 |
② | Cl2、FeBr2 | FeCl3、FeBr3 |
③ | MnO4- | Cl2、Mn2+ |
A.氧化性由强到弱顺序为MnO4->Cl2>Fe3+>Br2
B.第①组反应的氧化产物为O2
C.第②组反应中参加反应的Cl2与 FeBr2的物质的量之比为1:2
D.第③组反应中生成1mol Cl2,转移电子2mol
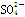 +Ba2++2OH-===BaSO4↓+Fe(OH)2↓
+Ba2++2OH-===BaSO4↓+Fe(OH)2↓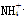 +Fe3++
+Fe3++ Pu作为热源材料。下列关于
Pu作为热源材料。下列关于 的亚硫酸钠溶液,则在此反应中X元素的低价态为
的亚硫酸钠溶液,则在此反应中X元素的低价态为