题目内容
 按要求完成下列问题:
按要求完成下列问题:(1)写出下列反应的化学方程式:
①乙烯通入到溴的四氯化碳溶液中:
②苯与浓硝酸、浓硫酸混和后加热至50℃~60℃发生反应:
(2)苯可以和浓硫酸发生取代反应生成苯磺酸(
 ),根据质量守恒定律,可判断出另一个反应产物为
),根据质量守恒定律,可判断出另一个反应产物为(3)石蜡油(主要是含17个碳原子以上的液态烷烃混合物)分解实验按照如图进行:
①碎瓷片的作用是
A.作反应物 B.积蓄热量 C.有催化功能 D.防止暴沸
②将石蜡油分解所得生成物通入到酸性高锰酸钾溶液中,现象是
考点:有机物的结构和性质,有机化学反应的综合应用,石油的裂化和裂解
专题:有机反应
分析:(1)①乙烯通入到溴的四氯化碳溶液中,发生加成反应生成1,2-二溴乙烷;
②苯与浓硝酸、浓硫酸混和后加热至50℃~60℃发生取代反应,生成硝基苯和水;
(2)苯可以和浓硫酸发生取代反应生成苯磺酸( ,同时生成水;
,同时生成水;
(3)①碎瓷片可防止暴沸、同时可加快分解速率;
②石蜡油分解产物中含乙烯,可被酸性高锰酸钾溶液氧化.
②苯与浓硝酸、浓硫酸混和后加热至50℃~60℃发生取代反应,生成硝基苯和水;
(2)苯可以和浓硫酸发生取代反应生成苯磺酸(
 ,同时生成水;
,同时生成水;(3)①碎瓷片可防止暴沸、同时可加快分解速率;
②石蜡油分解产物中含乙烯,可被酸性高锰酸钾溶液氧化.
解答:
解:(1)①乙烯通入到溴的四氯化碳溶液中,发生加成反应生成1,2-二溴乙烷,该反应为CH2=CH2+Br2→CH2BrCH2Br,
故答案为:CH2=CH2+Br2→CH2BrCH2Br;
②苯与浓硝酸、浓硫酸混和后加热至50℃~60℃发生取代反应,生成硝基苯和水,该反应为 ,
,
故答案为: ;
;
(2)苯可以和浓硫酸发生取代反应生成苯磺酸( ,发生取代反应,苯中被取代的H与硫酸中-OH结合,由质量守恒定律可知生成水H2O,故答案为:H2O;
,发生取代反应,苯中被取代的H与硫酸中-OH结合,由质量守恒定律可知生成水H2O,故答案为:H2O;
(3)①碎瓷片可防止暴沸、同时可加快分解速率,其作用为B、C,故答案为:BC;
②石蜡油分解产物中含乙烯,可被酸性高锰酸钾溶液氧化,则观察到酸性高锰酸钾溶液紫色褪去,故答案为:酸性高锰酸钾溶液紫色褪去.
故答案为:CH2=CH2+Br2→CH2BrCH2Br;
②苯与浓硝酸、浓硫酸混和后加热至50℃~60℃发生取代反应,生成硝基苯和水,该反应为
 ,
,故答案为:
 ;
;(2)苯可以和浓硫酸发生取代反应生成苯磺酸(
 ,发生取代反应,苯中被取代的H与硫酸中-OH结合,由质量守恒定律可知生成水H2O,故答案为:H2O;
,发生取代反应,苯中被取代的H与硫酸中-OH结合,由质量守恒定律可知生成水H2O,故答案为:H2O;(3)①碎瓷片可防止暴沸、同时可加快分解速率,其作用为B、C,故答案为:BC;
②石蜡油分解产物中含乙烯,可被酸性高锰酸钾溶液氧化,则观察到酸性高锰酸钾溶液紫色褪去,故答案为:酸性高锰酸钾溶液紫色褪去.
点评:本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重烯烃、苯的性质的考查,注意石蜡油分解产物中含乙烯,题目难度不大.

练习册系列答案
相关题目
下列装置或操作能达到实验目的是( )
A、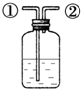 用排饱和食盐水法收集氯气,瓶内装饱和食盐水,氯气从①口进,②口出 |
B、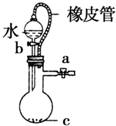 该装置中橡皮管的作用是能使水顺利流下 |
C、 除去苯中的己烷 |
D、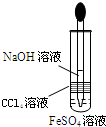 制备Fe(OH)2 |
下列变化可通过一步化学反应实现的是( )
| A、S→S03 |
| B、Al203→Al( OH)3 |
| C、Si02→H2SiO3 |
| D、Na2CO3→NaOH |

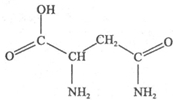 天冬酰胺(结构如图)在芦笋中含量丰富,具有提高身体免疫力的功效.
天冬酰胺(结构如图)在芦笋中含量丰富,具有提高身体免疫力的功效.