题目内容
10.下列说法正确的是( )| A. | 氢气、石油、煤、油脂都属于化石燃料 | |
| B. | 蔗糖及其水解产物均可发生银镜反应 | |
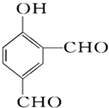
| C. | 分子式为(C6H10O5)n的淀粉和纤维素互为同分异构体 | |
| D. | 油脂在碱性条件下的水解反应又称为皂化反应 |
分析 A.石油、煤、天然气为化石燃料;
B.蔗糖及水解生成的果糖不含-CHO;
C.(C6H10O5)n中n不同;
D.油脂为高级脂肪酸甘油酯.
解答 解:A.石油、煤、天然气为化石燃料,而氢气、油脂不是,故A错误;
B.蔗糖及水解生成的果糖不含-CHO,只有水解生成的葡萄糖可发生银镜反应,故B错误;
C.(C6H10O5)n中n不同,则淀粉和纤维素互不是同分异构体,故C错误;
D.油脂为高级脂肪酸甘油酯,则油脂在碱性条件下的水解反应又称为皂化反应,故D正确;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意糖类、油脂的性质及应用,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.物质的量浓度相同的下列物质的水溶液,pH最小的是( )
| A. | Na2CO3 | B. | NH4Cl | C. | H2SO4 | D. | CH3COOH |
18.下列过程中不涉及氧化还原反应的是( )
| A. | 用葡萄酿制葡萄酒 | |
| B. | 夏季油脂变质 | |
| C. | 烹鱼时加入少量的料酒和食醋可减少腥味,增加香味 | |
| D. | 用新制氢氧化铜悬浊液检验病人是否患糖尿病 |
5. 乙醛在氧化铜催化剂的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示,试管A中装有40%的乙醛水溶液、氧化铜粉末;烧杯B中装有某液体).已知在60℃-80℃时用双链大气球鼓入空气即可发生乙醛的氧化反应,联系鼓入十几次反应基本完全.有关物质的沸点见下表:
乙醛在氧化铜催化剂的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示,试管A中装有40%的乙醛水溶液、氧化铜粉末;烧杯B中装有某液体).已知在60℃-80℃时用双链大气球鼓入空气即可发生乙醛的氧化反应,联系鼓入十几次反应基本完全.有关物质的沸点见下表:
请回答下列问题:
(1)试管A内在60℃-80℃时发生的主要反应的化学方程式为(注明反应条件)2CH3CHO+O2$→_{60℃-80℃}^{CuO}$2CH3COOH.
(2)如图所示在实验的不同阶段,需要调整温度计在试管A内的位置,在实验开始时温度计水银球的位置应在试管A的反应液中;目的是测反应液的温度;
当试管A内的主要反应完成后温度计水银球的位置应在试管A的支管口处.
(3)烧杯B的作用是使试管A内的反应液均匀受热发生反应,使生成的乙酸变成蒸气进入试管C,烧杯B内盛装的液体可以是乙二醇或甘油.
(写出一种即可,在题给物质中找);某同学认为试管C最好置于冰水浴中,其目的是有利于乙酸的冷凝收集.
(4)对C中产品进行蒸馏时,蒸馏烧瓶中装加入少量D,以出去其中含有的少量水.
A.浓硫酸 B.CaO C.CuSO4溶液 D.无水CaCL2
(5)以下区分乙酸精品和粗品的方法,合理的是B.
A.加入水观察实验现象
B.加入足量氢氧化钠溶液后,再加入银氨溶液,水浴加热观察实验现象
C.加入碳酸氢钠溶液,震荡后观察实验现象.
 乙醛在氧化铜催化剂的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示,试管A中装有40%的乙醛水溶液、氧化铜粉末;烧杯B中装有某液体).已知在60℃-80℃时用双链大气球鼓入空气即可发生乙醛的氧化反应,联系鼓入十几次反应基本完全.有关物质的沸点见下表:
乙醛在氧化铜催化剂的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示,试管A中装有40%的乙醛水溶液、氧化铜粉末;烧杯B中装有某液体).已知在60℃-80℃时用双链大气球鼓入空气即可发生乙醛的氧化反应,联系鼓入十几次反应基本完全.有关物质的沸点见下表:| 物质 | 乙醛 | 乙酸 | 甘油 | 乙二醇 | 水 |
| 沸点 | 20.8 | 117.9 | 290 | 197.2 | 100 |
(1)试管A内在60℃-80℃时发生的主要反应的化学方程式为(注明反应条件)2CH3CHO+O2$→_{60℃-80℃}^{CuO}$2CH3COOH.
(2)如图所示在实验的不同阶段,需要调整温度计在试管A内的位置,在实验开始时温度计水银球的位置应在试管A的反应液中;目的是测反应液的温度;
当试管A内的主要反应完成后温度计水银球的位置应在试管A的支管口处.
(3)烧杯B的作用是使试管A内的反应液均匀受热发生反应,使生成的乙酸变成蒸气进入试管C,烧杯B内盛装的液体可以是乙二醇或甘油.
(写出一种即可,在题给物质中找);某同学认为试管C最好置于冰水浴中,其目的是有利于乙酸的冷凝收集.
(4)对C中产品进行蒸馏时,蒸馏烧瓶中装加入少量D,以出去其中含有的少量水.
A.浓硫酸 B.CaO C.CuSO4溶液 D.无水CaCL2
(5)以下区分乙酸精品和粗品的方法,合理的是B.
A.加入水观察实验现象
B.加入足量氢氧化钠溶液后,再加入银氨溶液,水浴加热观察实验现象
C.加入碳酸氢钠溶液,震荡后观察实验现象.
2.设NA为阿伏加德罗常数,下列说法中正确的是( )
| A. | 17g氨气中所含原子数为NA | |
| B. | 2NA个二氧化碳分子的质量为44g | |
| C. | 2.4g金属镁与足量盐酸完全反应,失电子总数为0.2NA | |
| D. | 0.1mol/LNaCl溶液中,Na+与Cl-离子总数为0.2NA |
3.某化学兴趣小组要完成中和热的测定.
(1)实验桌上备有大烧杯、两个小烧杯、50mL量筒两个、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5mol•L-1盐酸、0.55mol•L-1 NaOH溶液,实验尚缺少的玻璃用品是温度计.
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?否(填“能”或“否”).
(3)他们记录的实验数据如下:
已知:Q=c•m•(t2-t1),反应后溶液的比热容c为4.18J•℃-1•g-1,各物质的密度均为1g•cm-3.
计算完成上表中△H=-56.8kJ/mol(保留到小数点后一位),中和热数值偏小的原因可能是分多次把NaOH溶液倒人盛有HCl小烧杯中(任填一条即可).
(4)若用KOH代替NaOH做实验,测定结果中和热数值无(填“有”或“无”)影响;若用醋酸代替HCl做实验,测定结果中和热数值偏小(填“偏大”、“偏小”或“无影响”).
(1)实验桌上备有大烧杯、两个小烧杯、50mL量筒两个、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5mol•L-1盐酸、0.55mol•L-1 NaOH溶液,实验尚缺少的玻璃用品是温度计.
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?否(填“能”或“否”).
(3)他们记录的实验数据如下:
| 实验用品 | 溶液温度 | 中和热 | |||
| t1 | t2 | △H | |||
| ① | 50mL0.55mol•L-1NaOH | 50mL.0.5mol•L-1HCl | 20℃ | 23.3℃ | |
| ② | 50mL0.55mol•L-1NaOH | 50mL.0.5mol•L-1HCl | 20℃ | 23.5℃ | |
计算完成上表中△H=-56.8kJ/mol(保留到小数点后一位),中和热数值偏小的原因可能是分多次把NaOH溶液倒人盛有HCl小烧杯中(任填一条即可).
(4)若用KOH代替NaOH做实验,测定结果中和热数值无(填“有”或“无”)影响;若用醋酸代替HCl做实验,测定结果中和热数值偏小(填“偏大”、“偏小”或“无影响”).