题目内容
已知硫酸溶液的质量分数越大时,其溶液的密度越大,将90%和10%的两种H2SO4溶液等体积混合后,溶液的质量分数为( )
| A、大于50% | B、等于50% |
| C、小于50% | D、无法确定 |
考点:溶液中溶质的质量分数及相关计算
专题:
分析:令质量分数分别为20%与80%的硫酸溶液的密度分别为xg/ml、yg/ml,硫酸溶液的密度随浓度增大而增大,所以x<y.假定体积为1ml,混合后溶质质量为混合前两溶液中溶质质量之和,混合后溶液质量为混合前溶液质量之和,根据质量分数定义用x、y表示出混合后的质量分数,结合密度关系判断.
解答:
解:设质量分数分别为10%与90%的硫酸溶液的密度分别为xg/ml、yg/ml;硫酸溶液的密度随浓度增大而增大,所以x<y.
假定体积为1ml,则10%硫酸溶液的质量为1ml×xg/ml=xg,溶质硫酸的质量为xg×10%;
90%的硫酸溶液的质量为1ml×yg/ml=yg,溶质硫酸的质量为yg×90%;
所以混合后硫酸的溶质质量分数=
=
=
,由于x<y,所以
>1,
所以90%-80%
>50%,
故选:A.
假定体积为1ml,则10%硫酸溶液的质量为1ml×xg/ml=xg,溶质硫酸的质量为xg×10%;
90%的硫酸溶液的质量为1ml×yg/ml=yg,溶质硫酸的质量为yg×90%;
所以混合后硫酸的溶质质量分数=
| 10%x+90%y |
| x+y |
10%+
| ||
1+
|
10%-90%+90%(1+
| ||
1+
|
| y |
| x |
所以90%-80%
| 1 | ||
1+
|
故选:A.
点评:本题考查溶液浓度的计算和大小比较,题目难度较大,注意硫酸的浓度越大,密度越大,并且解题规律是十分重要的.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
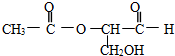 在有机物分子中,当碳原子连有4个不同的原子或原子团时,这种碳原子称为“手性碳原子”,凡具有一个手性碳原子的化合物一定具有光学活性.例如下图表示的有机物中含有一个手性碳原子,具有光学活性.当发生下列变化时,生成的有机物无光学活性的是( )
在有机物分子中,当碳原子连有4个不同的原子或原子团时,这种碳原子称为“手性碳原子”,凡具有一个手性碳原子的化合物一定具有光学活性.例如下图表示的有机物中含有一个手性碳原子,具有光学活性.当发生下列变化时,生成的有机物无光学活性的是( )| A、与新制的银铵溶液共热 |
| B、与甲酸酯化 |
| C、与金属钠发生置换反应 |
| D、与H2加成 |
某无色混合气体,可能含有CO、H2、SO2、Cl2、HCl中的一种或几种,把它们通过NaOH溶液,无明显现象;再通过红热的CuO粉末,粉末变成红色;最后通往AgNO3溶液中,无沉淀生成,原混合气体中( )
| A、肯定没有Cl2和HCl |
| B、CO和H2中至少有一种 |
| C、不能确定有无HCl、SO2 |
| D、肯定有SO2 |
 实验室常用如图所示装置测定某固体有机物A的分子组成,测定装置如图(铁架台、铁夹、酒精灯等未画出).下列说法正确的是( )
实验室常用如图所示装置测定某固体有机物A的分子组成,测定装置如图(铁架台、铁夹、酒精灯等未画出).下列说法正确的是( )| A、测定前要先通入纯氧气,再点燃试管B |
| B、装置C可测定有机物中碳的含量 |
| C、装置D可测定燃烧产物中水的质量 |
| D、该装置能测定所有有机物的分子组成 |
在治疗贫血的药物中,含有的主要成分是( )
| A、Na2CO3 |
| B、KCl |
| C、KIO3 |
| D、FeSO4 |
 生物质能是一种洁净、可再生能源.生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一.
生物质能是一种洁净、可再生能源.生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一.