题目内容
(11分)(1)据报道以硼氢化合物NaBH4(H的化合价为-1价)和H2O2作原料的燃料电池,可用作通信卫星电源。负极材料采用Pt/C,正极材料采用MnO2,其工作原理如图所示。

写出该电池放电时负极的电极反应式: 。
(2)火箭发射常以液态肼(N2H4)为燃料,液态过氧化氢为助燃剂。
已知:N2H4(l) + O2(g) = N2(g)+ 2H2O(l) △H = – 534 kJ·mol—1
H2O2(l)= H2O(l) + 1/2O2(g) △H = – 98.6 kJ·mol—1
写出常温下,N2H4(l) 与 H2O2(l)反应生成N2和H2O的热化学方程式 。
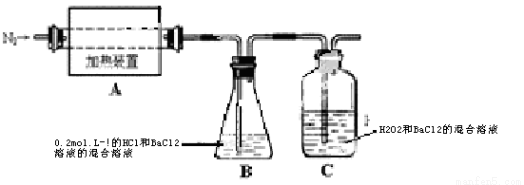
(3)O3可由臭氧发生器(原理如图所示)电解稀硫酸制得。

①图中阴极为 (填“A”或“B”)。
②若C处通入O 2,则A极的电极反应式为:
(4)向一密闭容器中充入一定量一氧化碳跟水蒸气发生反应CO(g)+H2O(g) CO2(g)+H2(g),下列情况下能判断该反应一定达到平衡状态的是____ _____(选填编号)。
CO2(g)+H2(g),下列情况下能判断该反应一定达到平衡状态的是____ _____(选填编号)。
A.v正(H2O) = v逆(H2)
B.容器中气体的压强不再发生改变
C.H2O的体积分数不再改变
D.容器中CO2和H2的物质的量之比不再发生改变
E.容器中气体的密度不再发生改变
(5)温度T1时,在一体积为2L的密闭容积中,加入0.4molCO2和0.4mol 的H2,反应中c(H2O)的变化情况如图所示

T1时反应CO(g)+H2O(g) CO2(g)+H2(g)第4分钟达到平衡。在第5分钟时向体系中同时再充入0.1molCO和0.1molH2(其他条件不变),请在右图中画出第5分钟到9分钟c(H2O)浓度变化趋势的曲线。
CO2(g)+H2(g)第4分钟达到平衡。在第5分钟时向体系中同时再充入0.1molCO和0.1molH2(其他条件不变),请在右图中画出第5分钟到9分钟c(H2O)浓度变化趋势的曲线。
(11分)(1)BH4- — 8e- + 8OH- = BO2- + 6H2O。(2分)
N2H4(l) + 2H2O2(l) = N2(g) + 4H2O(l) △H= -731.2 kJ /mol 。(2分)
(说明:△H数据、符号错,状态写错均不得分。)
(3)① A 。(1分)② O2 + 4H+ + 4e- = 2H2O 。(2分)
(4)AC 。(2分)(少选一个得1分,有错均不给分)
(5)(2分)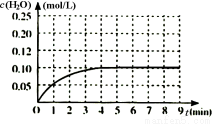
【解析】
试题分析:(1)根据原电池的装置图,可知负极是BH4发生氧化反应,B元素的化合价升高,与氢氧根离子结合生成BO2-和H2O,所以负极的电极反应式为BH4- — 8e- + 8OH- = BO2- + 6H2O;
(2)根据盖斯定律,将氧气消去,得N2H4(l) + 2H2O2(l) = N2(g) + 4H2O(l) △H=(–534 kJ·mol—1)+2×(–98.6 kJ·mol—1)=-731.2 kJ /mol;
(3)① 由图可知, B极产生氧气,则应是氢氧根离子放电,所以B是阳极,则A是阴极;
②若C处通入O 2,则阴极发生还原反应,氧气得到电子与氢离子结合为水,所以A极的电极反应式为O2 + 4H+ + 4e- = 2H2O;
(4)A.v正(H2O) = v逆(H2),正逆反应速率相等,符合化学平衡状态的特征,正确;B.容器中气体的压强不再发生改变的状态不是平衡状态,因为该反应的特点是气体物质的量不变的状态,所以压强一直不变,错误; C.平衡时,各物质的含量不再变化,所以H2O的体积分数不再改变 的状态是平衡状态,正确;D.容器中CO2和H2的物质的量之比不再发生改变的状态不一定是平衡状态,因为任何状态二氧化碳与水蒸气的物质的量之比都是1:1,保持不变,错误;E.因为气体的质量不变,容器的体积不变,则容器中气体的密度一直不变,所以气体密度不再发生改变的状态不是平衡状态,错误,答案选AC;
(5)在第5分钟时向体系中同时再充入0.1molCO和0.1molH2(其他条件不变),相当于增大压强,而压强的改变对平衡无影响,所以平衡不移动,c(H2O)仍为0.10mol/L,则图像为

考点:考查盖斯定律的应用,化学平衡状态的判断,电化学反应原理的应用

已知25℃,醋酸、次氯酸、碳酸、亚硫酸的电离平衡常数如下表,下列叙述正确的是
酸 | 醋酸 | 次氯酸 | 碳酸 | 亚硫酸 |
电离平衡常数 | K a=1.75×10-5 | K a=2.98×10-8 | Ka1=4.30×10-7 Ka2=5.61×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
A.25℃,等物质的量浓度的CH3COONa、NaClO、Na2CO3和Na2SO3 四种溶液中,碱性最强的是Na2CO3
B.将0.1 mol·L-1的醋酸加水不断稀释,所有离子浓度均减小
C.少量的SO2通入Ca(ClO)2溶液中反应的离子方程式为:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO
D.少量CO2通入NaClO溶液中反应的离子方程式为:CO2+H2O+2ClO-=CO32-+2HClO
一定温度下,在三个体积约为1.0L的恒容密闭容器中发生反应:
2CH3OH(g) CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
容器 编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
I | 387 | 0.20 | 0.080 | 0.080 |
Ⅱ | 387 | 0.40 | ||
Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
下列说法正确的是
A.该反应的正方应为吸热反应
B.达到平衡时,容器I中的CH3OH体积分数比容器Ⅱ中的小
C.容器I中反应达到平衡所需时间比容器Ⅲ中的长
D.若起始时向容器I中充入CH3OH 0.1mol、CH3OCH3 0.15mol和H2O 0.10mol,则反应将向正反应方向进行
 2Fe2O3?xH2O + 8H+,硫酸亚铁铵 溶液较硫酸亚铁溶液不易被氧气氧化,其原因是 。
2Fe2O3?xH2O + 8H+,硫酸亚铁铵 溶液较硫酸亚铁溶液不易被氧气氧化,其原因是 。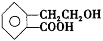 ,它可通过不同化学反应分别制得B、C、D和E四种物质。
,它可通过不同化学反应分别制得B、C、D和E四种物质。

 MnCl2+C12↑+2H2O.下列说法错误的是
MnCl2+C12↑+2H2O.下列说法错误的是