题目内容
实验室制Cl2的反应为4HCl(浓)+MnO2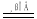 MnCl2+C12↑+2H2O.下列说法错误的是
MnCl2+C12↑+2H2O.下列说法错误的是
A.还原剂是HCl,氧化剂是MnO2
B.每生成1 molCl2,转移电子的物质的量为2 mol
C.每消耗1 molMnO2,起还原剂作用的HCl消耗4mol
D.生成的Cl2中,除含有一些水蒸气外,还含有HCl杂质
C
【解析】
试题分析:A、根据反应的化学方程式,Cl元素的化合价升高到0价,所以HCl作还原剂,Mn元素的化合价从+4价降低到+2价,所以二氧化锰作氧化剂,正确;B、每生成1 molCl2,则消耗1mol二氧化锰,则转移电子的物质的量为2 mol,正确;C、在反应中参加反应的HCl有一半作还原剂,所以每消耗1 molMnO2,参加反应的HCl为4mol,起还原剂作用的HCl消耗2mol,错误;D、因为浓盐酸乙挥发,所以生成的氯气中除水蒸气外还有少量的HCl气体,正确,答案选C。
考点:考查对氯气制取反应的分析,氧化还原反应的计算

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列实验操作、现象与结论对应关系正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 向盛有Fe(NO3)2溶液的试管中加入0.1 mol·L-1 H2SO4溶液 | 试管口出现红棕色气体 | 溶液中NO3-被 Fe2+还原为NO2 |
B | 向溶液中先滴加稀盐酸,再滴加BaCl2溶液 | 先滴加稀盐酸无现象,滴加BaCl2后出现白色沉淀 | 溶液中一定含有SO42- |
C | 在0.1mol·L-1CH3COONa溶液中,加两滴酚酞显浅红色,微热 | 红色加深 | 盐类水解是吸热反应 |
D | 向淀粉溶液中加入稀H2SO4,水浴加热几分钟,冷却后再加入新制Cu(OH)2悬浊液,加热 | 无砖红色沉淀生成 | 淀粉没有水解生成葡萄糖 |


 CO2(g)+H2(g),下列情况下能判断该反应一定达到平衡状态的是____ _____(选填编号)。
CO2(g)+H2(g),下列情况下能判断该反应一定达到平衡状态的是____ _____(选填编号)。

