��Ŀ����
��14�֣����������[(NH4)2Fe(SO4)2��6H2O]�������������ױ������������Ƿ�����ѧ����Ҫ���Լ��������ڴ������������������������ 500��ʱ��������������ȫ�ֽ⡣�ش��������⣺
��1����������笠�������������ȫ�ֽ⣬������������ԭ��Ӧ��������������FeO��Fe2O3��������������NH3��SO3��H2O��N2�� ��
��2��Ϊ����ֽ����ijɷݣ��������ʵ��װ�ý���ʵ�飬����A�е�������������ֽ���ȫ��
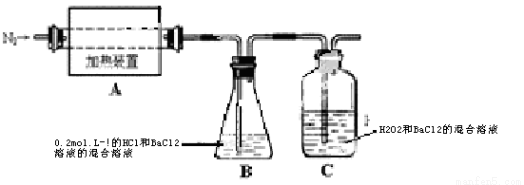
��A�й����ּ��Ƚϳ�ʱ���ͨ�뵪����Ŀ���� ��
��Ϊ��֤A�в������Ƿ���FeO����Ҫѡ�õ��Լ��� ��
A��KSCN��Һ B��ϡ���� C��Ũ���� D��KMnO4��Һ
��װ��B��BaCl2��Һ��������Ϊ�˼���ֽ�������Ƿ��� �������ɣ������и����壬�۲쵽������Ϊ ��
����A�зֽ������N2�����������ֻ��Fe2O3��Fe2O3�����ʵ���Ϊbmol��C�г������ʵ���Ϊamol����
b a������ڡ�����С�ڡ����ڡ���
��ʵ���У��۲쵽C���а�ɫ�������ɣ���C�з����ķ�ӦΪ �������ӷ���ʽ��ʾ����
��3����֪�������ӱ����������ķ�Ӧ�ǣ�4Fe2+ + O2 + (4+2x) H2O 2Fe2O3?xH2O + 8H+����������� ��Һ������������Һ���ױ�������������ԭ���� ��
2Fe2O3?xH2O + 8H+����������� ��Һ������������Һ���ױ�������������ԭ���� ��
��1��SO2 ��2����ʹ�ֽ������������B��C�б����ճ�� ��BD ��SO3 ��Һ�����
��С�ڢ�SO2+H2O2+Ba2+=BaSO4��+2H+ ��3�������������Һ��NH4+����ˮ������c��H+����������
����������ԭ��Ӧ�Ľ���
��������
�����������1����Ԫ�غ���Ԫ�ػ��ϼ����ߣ�������������ԭ��Ӧ�л��ϼ��������н������ϼ۽��͵�Ӧ������������������л�������SO2����2����A�й����ּ��Ƚϳ�ʱ���ͨ�뵪��Ŀ����ʹ�ֽ����ɵ�������BCװ������ȫ���գ���Ϊ��֤A�в������Ƿ���FeO��Ӧ������ϡ�����ܽ⣬Ȼ������KMnO4��Һ�����������ӣ���ѡBD����װ��B��BaC12��Һ��������Ϊ�˼���ֽ�������Ƿ���SO3�������ɣ������и����壬���������ᱵ��ɫ�������۲쵽�Ĺ���Ϊ��Һ����ǣ�
����A�зֽ������N2�����������ֻ��Fe2O3��Fe2O3�����ʵ���Ϊbmol��C�г������ʵ���Ϊamol�����ݻ��ϼ���������ȣ��͵Ļ��ϼۣ�2a�����������ߵĻ��ϼۣ�2b���͵����ߵĻ��ϼ�֮�ͣ���bС��a����C���а�ɫ�������ɣ�����ΪSO2��˫��ˮ������SO42-��SO42-����Ba2+��ϳɳ���BaSO4����C�з����ķ�ӦΪSO2+H2O2+Ba2+=BaSO4��+2H+����3�������������Һ������������Һ���ױ�������������Ϊ��Һ��笠�����ˮ�������ԣ�������Ũ����������������ԭ��Ӧ�ķ�����
���㣺̽��ʵ��

�±�������ͬ�¶����������һЩ���ݣ������ж���ȷ����
�� | HX | HY | HZ | ||
Ũ�ȣ�mol/L�� | 0.12 | 0.2 | 0.9 | 1 | 1 |
����� | 0.25 | 0.2 | 0.1 | 0.3 | 0.5 |
���볣�� | K1 | K2 | K3 | K4 | K5 |
A������ͬ�¶ȣ���HX�����ݿ���˵�������������Һ��Ũ��Խ�ͣ������Խ����K1��K2��K3=0.01
B������ʱ������NaZ��Һ�м�ˮ����c��Z-��/ [c��HZ��? c��OH-��]�ı�ֵ��С�������������ᣬ���ֵ���
C�������ʵ�����NaX��NaY��NaZ�Ļ�ϣ�c��X-��+c��Y-��-2c��Z-��=2c��HZ��-c��HX��-c��HY������c��Z-��<c��Y-��<c��X-��
D������ͬ�¶��£�K5��K4��K3
��ѧϰ�У����Ǿ���Ӧ�����Ʒ������������ȷ�����Ʒ�Ӧ�����ұ�Ҳ��ȷ����
AA | ��FeCl2��Һ�е�����ˮ 2Fe2�� + Cl2 �� 2Fe3�� + 2Cl�� | ��FeCl2��Һ�е����ˮ 2Fe2�� + I2 �� 2Fe3��+2I�� |
B | CO2ͨ��Ư����Һ�� CO2+ Ca2��+2ClO��+H2O=CaCO3��+ 2HClO | SO2ͨ��Ư����Һ�� SO2 +Ca2��+2ClO��+H2O��CaSO3��+2HClO |
C | ��Na2CO3��Һ�е���ϡHNO3 CO32�� �� 2H�� �� CO2���� H2O | ��Na2SO3��Һ�е���ϡHNO3 SO32�� +2H�� �� SO2��+H2O |
D | �����ʯ��ˮ��ͨ������CO2 ���� Ca2��+2OH�� +CO2 �� CaCO3��+ H2O | �����ʯ��ˮ��ͨ������SO2 ���� Ca2��+2OH�� +SO2 �� CaSO3��+H2O |


 2C(g)����H��0ѧ����
2C(g)����H��0ѧ����

 CO2(g)+H2(g)��������������жϸ÷�Ӧһ���ﵽƽ��״̬����____ _____��ѡ���ţ���
CO2(g)+H2(g)��������������жϸ÷�Ӧһ���ﵽƽ��״̬����____ _____��ѡ���ţ���

