题目内容
20.一定量的甲烷在O2不足的情况下燃烧,得到CO、CO2和H2O的总质量为14.4g,若其中水的质量为7.2g,则CO的质量是2.8g.分析 甲烷分子式可知C、H原子数目之比为1:4,根据原子守恒可知2n(CO)+2n(CO2)=n(H2O),而水的物质的量为:$\frac{7.2g}{18g/mol}$=0.4mol,所以甲烷的物质的量为0.2mol,则是$\left\{\begin{array}{l}{2n(CO)+2n(C{O}_{2})=0.4}\\{28n(CO)+44n(C{O}_{2})=14.4g-7.2g}\end{array}\right.$,解之得:$\left\{\begin{array}{l}{x=0.1mol}\\{y=0.1mol}\end{array}\right.$,由此分析解答.
解答 解:甲烷分子式可知C、H原子数目之比为1:4,根据原子守恒可知2n(CO)+2n(CO2)=n(H2O),而水的物质的量为:$\frac{7.2g}{18g/mol}$=0.4mol,所以甲烷的物质的量为0.2mol,则是$\left\{\begin{array}{l}{2n(CO)+2n(C{O}_{2})=0.4}\\{28n(CO)+44n(C{O}_{2})=14.4g-7.2g}\end{array}\right.$,解之得:$\left\{\begin{array}{l}{x=0.1mol}\\{y=0.1mol}\end{array}\right.$,所以CO的质量是0.1mol×28g/mol=2.8g,
故答案为:2.8g.
点评 本题考查混合物有关计算,关键是根据甲烷分子式确定水蒸气物质的量与一氧化碳、二氧化碳总的物质的量关系.

练习册系列答案
相关题目
10.下列解释实验事实的离子方程式正确的是( )
| A. | 硫酸亚铁在空气中被氧化:4Fe2++3O2+6H2O═4Fe(OH)3 | |
| B. | 向CH2Br-COOH中加入足量的NaOH溶液并加热:CH2Br-COOH+OH-$\stackrel{△}{→}$CH2Br-COO-+H2O | |
| C. | FeCl3溶液中通入SO2,溶液黄色褪去:2Fe3++SO2+2H2O═2Fe2++SO42-+4H+ | |
| D. | 碳酸钠溶液滴入酚酞变红:CO32-+2H2O?H2CO3+2OH- |
11.常温下,下列溶液中的微粒浓度关系正确的是( )
| A. | pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,c(H+)不相等 | |
| B. | pH=8.3的NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| C. | 0.1 mol AgCl和0.1 mol AgI混合后加入1 L水中,所得溶液中:c(Cl-)=c(I-) | |
| D. | 0.2 mol/L CH3COOH溶液与0.1 mol/L NaOH溶液等体积混合后所得溶液中:2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH) |
12.下列物质中含碳质量分数最高的是( )
| A. | 苯 | B. | 辛烯 | C. | 辛烷 | D. | 十六烷 |
12.某均匀混合的白色粉末可能含有下列7种常见物质中的某4种:NaCl、BaCl2、Mg(NO3)2、K2CO3、CuSO4、NaHCO3、X,混合物中各成分的物质的量相等,且所含阴、阳离子数目之比为3:2,某同学做了以下实验,部分现象没有描述.根据所提供的实验现象,下列对该白色粉末的判断正确的是( )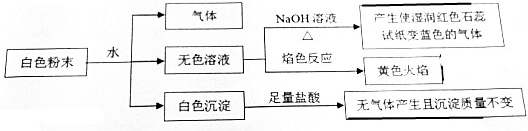

| A. | 一定含有BaCl2、Mg(NO3)2、NaHCO3、X,且X是NH4HSO4 | |
| B. | 一定不含K2CO3、CuSO4,X是NH4Al(SO4)2 | |
| C. | 一定含有BaCl2、NaHCO3、X且X是NH4AlO2,另一种为NaCl和Mg(NO3)2中的任一种 | |
| D. | 一定含有NaCl、BaCl2、NaHCO3和X,当X不能确定是什么物质 |
13.某溶液中可能含有物质的量浓度相等的下列离子中的几种:Fe3+、Cu2+、Na+、SO42-、CO32-、NO3-、Cl-、I-,取上述溶液少量分别进行如下实验:
①一份中加入少量锌粉后,固体溶解、溶液颜色有变化,但无其它现象产生
②一份加入BaCl2溶液后得到白色沉淀,下列有关判断正确的是( )
①一份中加入少量锌粉后,固体溶解、溶液颜色有变化,但无其它现象产生
②一份加入BaCl2溶液后得到白色沉淀,下列有关判断正确的是( )
| A. | 溶液中只含Fe3+、SO42-、Cl- | |
| B. | 溶液中只含Cu2+、SO42- | |
| C. | 需要利用焰色反应才能确定有无Na+ | |
| D. | 溶液中肯定没有I-,但无法确定有无Cl- |