题目内容
下列反应中,能用H++OH-=H2O表示的是( )
| A、NaOH溶液和CO2的反应 |
| B、Ba(OH)2溶液和稀H2SO4的反应 |
| C、NaOH溶液和盐酸的反应 |
| D、氢氧化铜和稀H2SO4的反应 |
考点:离子方程式的书写
专题:离子反应专题
分析:离子方程式“H++OH-=H2O”表示强酸与可溶性强碱生成可溶性盐的中和反应,并且溶液中仅存在H+和OH-的反应,据此对各选项进行判断.
解答:
解:A、氢氧化钠和二氧化碳反应生成碳酸钠和水,反应的离子方程式为:CO2+2OH-=CO32-+H2O,不能用H++OH-=H2O表示,故A错误;
B、Ba(OH)2溶液和稀H2SO4的反应生成的硫酸钡是难溶解的物质,反应的离子方程式为:2H++2OH-+SO42-+Ba2+═BaSO4↓+2H2O,不能用H++OH-=H2O表示,故B错误;
C、氢氧化钠是强碱,盐酸是强酸,生成的氯化钠是易溶于水的盐,能用H++OH-=H2O表示,故C正确;
D、Cu(OH)2难溶于水,与稀H2SO4的反应的离子方程式为:Cu(OH)2+2H+=Cua2++2H2O,不能用H++OH-=H2O表示,故D错误;
故选C.
B、Ba(OH)2溶液和稀H2SO4的反应生成的硫酸钡是难溶解的物质,反应的离子方程式为:2H++2OH-+SO42-+Ba2+═BaSO4↓+2H2O,不能用H++OH-=H2O表示,故B错误;
C、氢氧化钠是强碱,盐酸是强酸,生成的氯化钠是易溶于水的盐,能用H++OH-=H2O表示,故C正确;
D、Cu(OH)2难溶于水,与稀H2SO4的反应的离子方程式为:Cu(OH)2+2H+=Cua2++2H2O,不能用H++OH-=H2O表示,故D错误;
故选C.
点评:本题考查离子方程式的书写,题目难度中等,注意判断离子方程式的正误时要注意:①根据物质的性质判断反应是否符合实际,②难溶物或氧化物要写成化学式.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
化学电池可以直接将化学能转化为电能,化学电池的本质是( )
| A、化合价的升降 |
| B、电子的转移 |
| C、氧化还原反应 |
| D、电能的储存 |
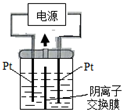 电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开.在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅.已知:3I2+6OH-═IO3-+5I-+3H2O,下列说法不正确的是( )
电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开.在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅.已知:3I2+6OH-═IO3-+5I-+3H2O,下列说法不正确的是( )| A、右侧发生的电极方程式:2H2O+2e-═H2↑+2OH- |
| B、电解结束时,右侧溶液中含有IO3- |
| C、电解槽内发生反应的总化学方程式KI+3H2O═KIO3+3H2 |
| D、如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总化学方程式不变 |
已知下列反应能够发生:
①2Fe2++Br2=2Fe3++2Br-
②2Fe3++2I-=2Fe2++I2
③2MnO4-+16H++10Br-=2Mn2++5Br2+8H2O
④I2+SO2+2H2O=4H++SO42-+2I-
据此,判断出氧化性由强到弱的正确顺序是( )
①2Fe2++Br2=2Fe3++2Br-
②2Fe3++2I-=2Fe2++I2
③2MnO4-+16H++10Br-=2Mn2++5Br2+8H2O
④I2+SO2+2H2O=4H++SO42-+2I-
据此,判断出氧化性由强到弱的正确顺序是( )
| A、MnO4->Fe3+>Br2>I2>SO2 |
| B、MnO4->Br2>Fe3+>I2>SO2 |
| C、MnO4->Br2>Fe3+>SO2>I2 |
| D、Br2>MnO4->Fe3+>I2>SO2 |
心酮胺是治疗冠心病的药物.它具有如下结构简式:下列关于心酮胺的描述,错误的是( )


| A、可以在催化剂作用下和溴反应 |
| B、可以在碱性条件下发生水解反应 |
| C、能够使酸性高锰酸钾溶液褪色 |
| D、可以和浓硫酸与浓硝酸的混合液反应 |
下列氯化物中,不能用金属单质和氯气直接反应制得的是( )
| A、CuCl2 |
| B、FeCl2 |
| C、MgCl2 |
| D、NaCl |
