题目内容
7.除去CO2中混有的少量SO2气体,最好选用的试剂是( )| A. | 澄清石灰水 | B. | 品红溶液 | C. | 溴水 | D. | 饱和NaHCO3溶液 |
分析 CO2和SO2都为酸性气体,都可与强碱性溶液反应,SO2具有还原性,除去CO2中的SO2,可用强氧化性物质或饱和NaHCO3溶液,以此解答.
解答 解:A.二者都可与石灰水反应生成沉淀,不能用于除杂,故A错误;
B.二氧化硫可与品红反应,但浓度未知,不一定能完全除去杂质,故B错误;
C.溴水可氧化二氧化硫,但溴易挥发,易引入溴蒸气杂质,故C错误;
D.SO2可与饱和NaHCO3溶液反应生成CO2,但CO2不反应,可用于除杂,故D正确.
故选D.
点评 本题考查物质的分离和提纯,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质的异同,除杂时不能引入新的杂质,难度不大.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案
相关题目
18.下述实验能达到预期目的是( )
| 编号 | 实验内容 | 实验目的 |
| A | 将CO2(含HC1杂质)通入饱和NaHCO3溶液中 | 除去HC1 |
| B | 向做完银镜反应后的试管中加入稀氨水 | 除去试管内残留物 |
| C | 向食盐溶液中滴加少量淀粉溶液 | 鉴别真假碘盐 |
| D | 将少量FeC12试样加水溶解,加稀硝酸酸化,再滴加KSCN溶液 | 检验FeCl2试样是否变质 |
| A. | A | B. | B | C. | C | D. | D |
2.下面关于 SiO2晶体网状结构的叙述正确的是( )
| A. | 存在四面体结构单元,O 处于中心,Si 处于 4 个顶角 | |
| B. | 最小的环上,有 3 个 Si 原子和 3 个 O 原子 | |
| C. | 最小的环上,Si 和 O 原子数之比为 1:2 | |
| D. | 最小的环上,有 6 个 Si 原子和 6 个 O 原子 |
12.下列反应中,改变反应物用量或浓度,不会改变反应产物的是( )
| A. | 铁在硫蒸气中燃烧 | B. | SO2通入石灰水 | ||
| C. | 氯气通入KI溶液 | D. | H2SO4中加入铁粉 |
19. 用石墨作电极电解KCl和CuSO4(等体积混合)混合溶液,电解过程中溶液pH随时间t的变化如图所示,下列说法正确的是( )
用石墨作电极电解KCl和CuSO4(等体积混合)混合溶液,电解过程中溶液pH随时间t的变化如图所示,下列说法正确的是( )
 用石墨作电极电解KCl和CuSO4(等体积混合)混合溶液,电解过程中溶液pH随时间t的变化如图所示,下列说法正确的是( )
用石墨作电极电解KCl和CuSO4(等体积混合)混合溶液,电解过程中溶液pH随时间t的变化如图所示,下列说法正确的是( )| A. | ab段H+被还原,溶液的pH 增大 | |
| B. | cd 段相当于电解水 | |
| C. | c点时加人适量CuCl2固体,电解液可恢复原来浓度 | |
| D. | 原溶液中KCl和CuSO4的物质的量浓度之比为2:1 |
16.下列说法不正确的是( )
| A. | O2和O3互为同素异形体 | |
| B. | ${\;}_{1}^{1}$H、${\;}_{1}^{2}$H和${\;}_{1}^{3}$H互为同位素 | |
| C. | CH2═CH2和 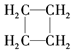 互为同系物 互为同系物 | |
| D. | 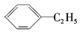 和 和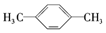 互为同分异构体 互为同分异构体 |
 钴、镍与铁是同族元素,主要化合价均为+2、+3价,它们的单质及化合物的性质有很多相似之处.试回答下列问题:
钴、镍与铁是同族元素,主要化合价均为+2、+3价,它们的单质及化合物的性质有很多相似之处.试回答下列问题: