题目内容
10.取代反应是有机化学中一类重要的反应,下列反应属于取代反应的是( )| A. | 丙烷与氯气在光照的作用下的反应 | B. | 乙烯与溴的四氯化溶液的反应 | ||
| C. | 乙烯与水的反应 | D. | 乙烯自身生成聚乙烯的反应 |
分析 根据发生的化学反应及反应的化学方程式进行判断,并注意利用反应条件来判断发生的化学反应.
解答 解:A、丙烷能与氯气在光照的作用下发生取代反应得到氯丙烷,故A正确;
B、乙烯能与溴的四氯化碳溶液中的溴发生加成反应生成溴乙烷,故B错误;
C、乙烯能与水发生加成反应得到乙醇,故C正确;
D、乙烯能通过自身加聚反应生成聚乙烯,故D正确;
故选A.
点评 本题主要考查了反应类型的判断,熟练掌握有机物的性质和反应机理是解题关键,难度不大.

练习册系列答案
 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案
相关题目
20.下列各组混合物中,可以用分液漏斗分离的是( )
| A. | 溴乙烷和水 | B. | 苯酚和乙醇 | C. | 酒精和水 | D. | 乙醛和苯 |
1.下列有关物质用途的说法中,不正确的是( )
| A. | 四氯化碳可做有机溶剂 | |
| B. | 可用工业酒精勾兑白酒 | |
| C. | 甲烷是清洁高效的燃料 | |
| D. | 用二氯甲烷只有一种结构证明甲烷空间结构是正四面体 |
18.下列粒子的结构示意图中,表示钠离子( )
| A. | 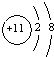 | B. | 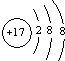 | C. | 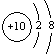 | D. | 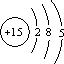 |
5.有人设计出利用CH4和O2反应,用铂电极在KOH溶液中构成原电池.电池的总反应类似于CH4在O2中燃烧的反应,则下列说法中正确的是( )
| A. | 每消耗l mol CH4可以向外电路提供8 mol e- | |
| B. | 负极上CH4失去电子,电极反应式为CH4+10OH--8e-═CO32-+7H2O | |
| C. | 电池放电时,正极附近的pH不断降低 | |
| D. | 电池放电时,溶液中的OH-向正极移动 |
15.在Na2CO3和HCl反应的下列各组实验中,反应速率最快的一组是( )
| 组号 | 温度(℃) | Na2CO3浓度(mol/L) | HCl浓度(mol/L) |
| A | 0 | 0.1 | 0.1 |
| B | 20 | 0.1 | 0.1 |
| C | 40 | 0.1 | 0.2 |
| D | 40 | 0.2 | 0.2 |
| A. | A | B. | B | C. | C | D. | D |
2.CoCl2•6H2O是一种饲料营养强化剂.以含钴单质废料(含少量Fe、Al等杂质)制取CoCl2•6H2O的一种新工艺流程如图:
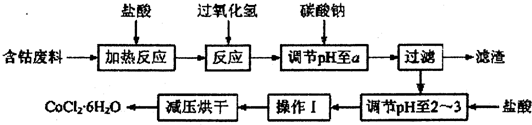
已知:
①CoCl2•6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴.
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
请回答下列问题:
(1)钴与盐酸反应的化学方程式为Co+2HCl=CoCl2+H2↑.
(2)流程中加入碳酸钠调节pH至a,a的范围是5.2~7.6;滤渣中含有的Al(OH)3是良好的阻燃剂,其原理是Al(OH)3受热分解时吸收大量的热,使环境温度下降;同时生成的耐高温、稳定性好的Al2O3覆盖在可燃物表面,阻燃效果更佳;加盐酸调节pH至2~3的目的是抑制Co2+的水解,防止在后续的操作中形成Co(OH)2杂质.
(3)操作Ⅰ包含3个基本实验操作,它们是蒸发浓缩、冷却结晶和过滤.
(4)制得的CoCl2•6H2O需减压烘干的原因是降低烘干温度,防止产品分解.
(5)为测定产品中CoCl2•6H2O含量,某同学将119g样品溶于水形成100ml溶液,取25mL于烧杯中加入足量的AgNO3溶液,过滤,并将沉淀烘干后称得质量为28.7g,计算产品中CoCl2•6H2O含量为80%.(已知:CoCl2•6H2O化学式量为238,AgCl为143.5,假设杂质不与AgNO3溶液反应,结果保留两位有效数字)

已知:
①CoCl2•6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴.
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀 | 4.1 | 9.7 | 9.2 | 5.2 |
(1)钴与盐酸反应的化学方程式为Co+2HCl=CoCl2+H2↑.
(2)流程中加入碳酸钠调节pH至a,a的范围是5.2~7.6;滤渣中含有的Al(OH)3是良好的阻燃剂,其原理是Al(OH)3受热分解时吸收大量的热,使环境温度下降;同时生成的耐高温、稳定性好的Al2O3覆盖在可燃物表面,阻燃效果更佳;加盐酸调节pH至2~3的目的是抑制Co2+的水解,防止在后续的操作中形成Co(OH)2杂质.
(3)操作Ⅰ包含3个基本实验操作,它们是蒸发浓缩、冷却结晶和过滤.
(4)制得的CoCl2•6H2O需减压烘干的原因是降低烘干温度,防止产品分解.
(5)为测定产品中CoCl2•6H2O含量,某同学将119g样品溶于水形成100ml溶液,取25mL于烧杯中加入足量的AgNO3溶液,过滤,并将沉淀烘干后称得质量为28.7g,计算产品中CoCl2•6H2O含量为80%.(已知:CoCl2•6H2O化学式量为238,AgCl为143.5,假设杂质不与AgNO3溶液反应,结果保留两位有效数字)
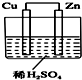 如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是( )
如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是( )