题目内容
11.下列物质中:A.KI固体 B.乙醇 C.Cl2 D.CaCO3固体 E.H2SO4 F.Mg(OH)2 G.石墨 H.CH3COOH
(1)属于非电解质的是B(填字母代号,下同),属于强电解质的是ADE,属于弱电解质的是FH.它们的电离方程式是Mg(OH)2?Mg2++2OH-;CH3COOH?CH3COO-+H+
(2)能直接导电的是G,水溶液能导电的是AEH.
分析 (1)水溶液中或熔融状态下导电的化合物为电解质,
水溶液中和熔融状态下都不导电的化合物为非电解质,
水溶液中完全电离的电解质为强电解质,水溶液中部分电离的电解质为弱电解质,
(2)物质能否导电与物质中是否含有自由移动的带电荷的微粒有关.需要注意的是:是否有“自由移动”的带电荷的微粒.溶液能够导电是因为溶液中含有自由移动的离子.溶液不导电是因为溶液中没有自由移动的离子.
解答 解:A.KI固体不能导电,溶于水能导电,属于电解质中的强电解质;
B.乙醇不能电离,不能导电,属于非电解质; C.Cl2 是单质不是电解质,不能导电;
D.CaCO3固体不能导电,熔融状态下导电,完全电离属于强电解质;
E.H2SO4 不能导电,溶于水完全电离是强电解质;
F.Mg(OH)2 不能导电,熔融状态部分电离导电,属于弱电解质;
G.石墨导电,是碳的单质不是电解质;
H.CH3COOH不能导电,水溶液中部分电离导电,属于弱电解质;
(1)属于非电解质的是B,属于强电解质的是ADE,属于弱电解质的是FH,它们的电离方程式是Mg(OH)2?Mg2++2OH-;CH3COOH?CH3COO-+H+,
故答案为:B;ADE; FH;Mg(OH)2?Mg2++2OH-;CH3COOH?CH3COO-+H+;
(2)能直接导电的是G,水溶液能导电的是AEH,
故答案为:G;AEH.
点评 本题考查了物质分类、电解质、非电解质、强电解质、弱电解质概念的理解应用,注意导电性的分析判断,题目难度不大.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
1.下列仪器的使用、实验药品选择或实验现象描述正确的是( )
| A. | 物质的分离提纯方法之一为“筛分”,如:胶体--渗析法提纯,浊液--过滤分离,本质上就是依据所分离粒子的直径大小选择具有合适孔径的“筛子” | |
| B. | 容量瓶、量筒和滴定管上都标有使用温度,容量瓶无“0”刻度,量筒和滴定管有“0”刻度;使用时滴定管水洗后还需润洗,但容量瓶水洗后不用润洗 | |
| C. | 工业上电解饱和食盐水时,为了阻止产物相互之间反应,往往用阴离子交换膜把阳极和阴极隔开 | |
| D. | 室温下,浓度均为0.1 mol•L-1Na2S2O3和H2SO4溶液,各取5 mL、10 mL的Na2S2O3溶液分别与10 mL的H2SO4溶液混合反应,可验证Na2S2O3浓度对反应速率的影响 |
2.若烷烃CH3CH2CH(CH3)CH(CH3)CH2CH3是烯烃与氢气的加成产物,烯烃可能的结构有a种,若该烷烃是炔烃与氢气的加成产物,炔烃可能的结构有b种,则a、b分别等于( )
| A. | 7、2 | B. | 7、1 | C. | 4、2 | D. | 4、1 |
19.某有机物1.8g在氧气中完全燃烧,只生成2.64g CO2和1.08H2O,下列说法正确的是( )
| A. | 该有机物仅含有碳、氢两种元素 | |
| B. | 该有机物中碳、氢原子的个数比是1:1 | |
| C. | 该有机物中一定含有氧元素 | |
| D. | 可以确定出该有机物的分子式 |
6.${\;}_{92}^{235}$U是重要的核工业原料,下列关于${\;}_{92}^{235}$U说法正确的是( )
| A. | ${\;}_{92}^{235}$U原子核中含有92个中子 | B. | ${\;}_{92}^{235}$U原子核外有143个电子 | ||
| C. | ${\;}_{92}^{235}$U的质量数为92 | D. | ${\;}_{92}^{235}$U与${\;}_{92}^{238}$U互为同位素 |
3.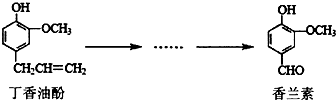 香兰素是重要的香料之一,它可由丁香油酚经多步反应合成(见如图).有关上述两种化合物的说法不正确的是( )
香兰素是重要的香料之一,它可由丁香油酚经多步反应合成(见如图).有关上述两种化合物的说法不正确的是( )
 香兰素是重要的香料之一,它可由丁香油酚经多步反应合成(见如图).有关上述两种化合物的说法不正确的是( )
香兰素是重要的香料之一,它可由丁香油酚经多步反应合成(见如图).有关上述两种化合物的说法不正确的是( )| A. | 在丁香油酚分子中至少有12个原子共平面 | |
| B. | 常温下,1mol丁香油酚可与2molBr2反应 | |
| C. | 1moI香兰素最多能与4mol氢气发生加成反应 | |
| D. | 可用酸性KMnO4溶液检验丁香油酚中是否含有碳碳双键 |
4.下列各图所表示的“一个反应过程”符合放热反应的是( )
| A. |  | B. |  | C. |  | D. |  |
 .
.