题目内容
11.下列变化过程中,不能肯定是吸热过程的是( )| A. | 化学反应 | B. | 水的电离 | C. | 盐的水解 | D. | 干冰的升华 |
分析 反应放热还是吸热主要取决于反应物和生成物所具有的总能量的相对大小,任何化学反应均伴随着能量的变化,电离、水解是吸热过程,物质大三态变化也有能量的变化,据此解答即可.
解答 解:A.任何化学反应均伴随着能量的变化,可能是放热也可能是吸热,故A符合题意;
B.水的电离属于吸热过程,故B不符合题意;
C.盐类的水解属于吸热过程,故C不符合题意;
D.干冰的升华属于吸热过程,故D不符合题意,
故选A.
点评 本题考查化学反应中能量的变化,难度较小,旨在考查学生对基础知识的识记,注意基础知识的积累掌握.

练习册系列答案
相关题目
2.S-诱抗素制剂的分子结构如图,下列关于该分子说法正确的是( )


| A. | 含有碳碳双键、羟基、羰基、羧基 | B. | 含有苯环、羟基、羰基、羧基 | ||
| C. | 含有羟基、羰基、羧基、酯基 | D. | 含有碳碳双键、苯环、羟基、羰基 |
19.一定温度和压强下,下列各可逆反应达到化学平衡状态,各反应有如图所示的对应关系:

(1)N2(g)+3H2(g)?2NH3(g)△H<0(曲线Ⅰ)
(2)H2(g)+I2(g)?2HI(g)△H>0(曲线Ⅱ)
(3)2SO3(g)?2SO2(g)+O2(g)△H>0(曲线Ⅲ)
则下列y轴的表达意义均符合上述三个平衡状态的是( )

(1)N2(g)+3H2(g)?2NH3(g)△H<0(曲线Ⅰ)
(2)H2(g)+I2(g)?2HI(g)△H>0(曲线Ⅱ)
(3)2SO3(g)?2SO2(g)+O2(g)△H>0(曲线Ⅲ)
则下列y轴的表达意义均符合上述三个平衡状态的是( )
| A. | 平衡混合气的平均相对分子质量 | |
| B. | 平衡混合气中一种反应物的浓度 | |
| C. | 平衡混合气中一种生成物的体积分数 | |
| D. | 平衡混合气中一种反应物的体积分数 |
16.设NA为阿伏加德罗常数,下列叙述中正确的是( )
| A. | 标准状况下,11.2L苯中含有C-H键的数目为3NA | |
| B. | 常温下,1.0LPH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA | |
| C. | 常温下,56g铁片投入足量浓H2SO4中生成NA个SO2分子 | |
| D. | 电解饱和食盐水,阳极产生22.4L气体时,电路中通过的电子数目为2NA |
3.常温下,将CO2缓慢通入一定体积的NaOH溶液中,溶液的pH随通入CO2(标准状况)的变化曲线如图所示(忽略CO2的溶解),则下列说法中正确的是( )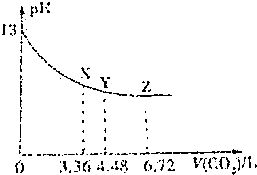

| A. | 该NaOH溶液的浓度为0.1mol/L,体积为6L | |
| B. | X、Y、Z三点对应的溶液中离子的种类不同 | |
| C. | Y点对应的融资中离子浓度关系为:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) | |
| D. | Y点对应的溶液中存在着:c(Na+)=2c(HCO3-)+c(OH-) |

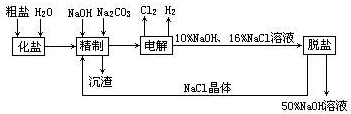
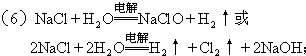 .
.