题目内容
下列叙述中正确的是( )
| A、两种微粒,若核外电子排布完全相同,其化学性质也一定相同 |
| B、凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布 |
| C、两种原子若核外电子排布相同,则一定属于同种元素 |
| D、存在两种质子数和电子数均相同的阳离子和阴离子 |
考点:原子核外电子排布,原子结构与元素的性质
专题:
分析:A、核外电子排布相同的粒子,化学性质不一定相同;
B、H+核外没有电子;
C、两种原子若核外电子排布相同,则质子数一定相同;
D、存在两种质子数和电子数均相同离子不可能为阳离子和阴离子.
B、H+核外没有电子;
C、两种原子若核外电子排布相同,则质子数一定相同;
D、存在两种质子数和电子数均相同离子不可能为阳离子和阴离子.
解答:
解:A、核外电子排布相同的粒子,化学性质不一定相同,如Na+和OH-,故A错误;
B、H+核外没有电子,与稀有气体元素原子的核外电子排布不同,故B错误;
C、两种原子若核外电子排布相同,则质子数一定相同,一定为同种元素,故C正确;
D、阳离子的质子数大于电子数,阴离子的质子数小于电子数,如电子数相同,则质子数一定不同,故D错误;
故选C.
B、H+核外没有电子,与稀有气体元素原子的核外电子排布不同,故B错误;
C、两种原子若核外电子排布相同,则质子数一定相同,一定为同种元素,故C正确;
D、阳离子的质子数大于电子数,阴离子的质子数小于电子数,如电子数相同,则质子数一定不同,故D错误;
故选C.
点评:本题考查原子结构和元素的性质,题目难度中等,本题易错点为C,注意阳离子的质子数大于电子数,阴离子的质子数小于电子数的关系.

练习册系列答案
相关题目
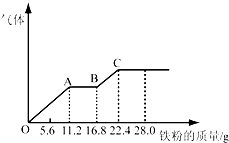 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示.下列分析或结果不正确的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示.下列分析或结果不正确的是( )| A、混合酸中HNO3物质的量浓度为2mol?L-1 |
| B、OA段产生的是NO,AB段的反应为Fe+2Fe3+═3Fe2+,BC段产生氢气 |
| C、原混合酸中H2SO4物质的量为0.4 mol |
| D、第二份溶液中最终溶质为FeSO4 |
由Na2O、Na2O2、Na2CO3、NaHCO3、NaCl中的某几种组成的混合物,向混合物中加入足量盐酸,有气体逸出,将放出的气体通过过量的NaOH溶液后,气体体积有所减小,或将上述混合物在空气中充分加热,也有气体放出,且加热后残留固体物质的质量比加热前有所增加,下列推断正确的是( )
| A、混合物中一定含有Na2O、Na2O2、和NaHCO3 |
| B、混合物中一定不含Na2CO3和NaCl |
| C、混合物中可能含有Na2O和NaCl |
| D、混合物中一定不含Na2O2和NaCl |
下列根据实验现象所得出的结论中,一定正确的是( )
| A、无色试液加入氯化钡溶液有白色沉淀,结论:试液中含有SO42- |
| B、无色溶液加入硝酸银溶液有白色沉淀,结论:试液中含有Cl- |
| C、无色试液加入Na2CO3溶液产生白色沉淀,结论:试液中含Ca2+ |
| D、某气体能使湿润的红色石蕊试纸变蓝,结论:该气体为NH3 |
MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如图所示.下列叙述中正确的是( )

| A、常温下,醋酸和ROH溶液的pH之和为14时,等体积混合,所得溶液呈碱性 |
| B、在x点时,ROH完全电离 |
| C、在x点,c(M+)>c(R+) |
| D、稀释前,c(ROH)=10c(MOH) |