题目内容
已知P4 (s,白磷)+5O2 (g)=P4O10(s);△H1=-2983.2KJ/mol,P(s,红磷)+
(g)=
P4O10(s);△H2=-738.5KJ/mol试应用盖斯定律写出白磷转化为红磷的热化学方程式: .
| 5 |
| 4 |
| 1 |
| 4 |
考点:用盖斯定律进行有关反应热的计算
专题:
分析:根据盖斯定律可以计算化学反应的焓变,进而书写热化学方程式.
解答:
解:红磷转化为白磷的化学方程式为:4P(s、红磷)=P4(s、白磷),可以看成是下列两个反应方程式的和:P4O10(s)=P4(s、白磷)+5O2(g);△H=2983.2kJ?mol-1
;4P(s、红磷)+5O2(g)=P4O10(s);△H=-738.5×4kJ?mol-1=-2954kJ?mol-1;
根据盖斯定律,红磷转化为白磷4P(s、红磷)=P4(s、白磷)的△H=2983.2kJ/mol-2954kJ?mol-1=29.2KJ/mol,
故答案为:4P(s、红磷)=P4(s、白磷)△H=+29.2KJ/mol.
;4P(s、红磷)+5O2(g)=P4O10(s);△H=-738.5×4kJ?mol-1=-2954kJ?mol-1;
根据盖斯定律,红磷转化为白磷4P(s、红磷)=P4(s、白磷)的△H=2983.2kJ/mol-2954kJ?mol-1=29.2KJ/mol,
故答案为:4P(s、红磷)=P4(s、白磷)△H=+29.2KJ/mol.
点评:本题考查学生利用盖斯定律来计算化学反应的焓变这一知识,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目
德、法、美及波兰等多国科学家组成的科研小组合成了非常罕见的4526Fe原子,有关4526Fe的说法正确的是( )
| A、它是一种新元素 |
| B、4526Fe与5626Fe互为同素异形体 |
| C、它是一种新核素 |
| D、这是铁原子发生衰变放出两个质子形成的核素 |
实验室里需用480mL 0.1mol?L-1的硫酸铜溶液,现用容量瓶进行配制,以下操作确的( )
| A、称取7.68g硫酸铜,加入500mL水 |
| B、称取12.0g胆矾配成500mL溶液 |
| C、称取8.0g硫酸铜配成500mL溶液 |
| D、称取12.5g胆矾配成480mL溶液 |
两种金属的混合粉末25g,与足量盐酸充分反应后,得到标准状况下的氢气11.2L.下列各组金属不可能的是( )
| A、Mg和Zn |
| B、Mg和Fe |
| C、A1和Na |
| D、A1和Cu |
下列叙述中正确的是( )
| A、两种微粒,若核外电子排布完全相同,其化学性质也一定相同 |
| B、凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布 |
| C、两种原子若核外电子排布相同,则一定属于同种元素 |
| D、存在两种质子数和电子数均相同的阳离子和阴离子 |
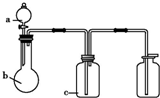 图中a、b、c表示相应仪器中加入的试剂,可用下图装置制取、净化、收集的
图中a、b、c表示相应仪器中加入的试剂,可用下图装置制取、净化、收集的气体是( )
| 编号 | 气体 | a | b | c |
| A | NH3 | 浓氨水 | 生石灰 | 碱石灰 |
| B | CO2 | 盐酸 | 碳酸钙 | 饱和NaHCO3溶液 |
| C | NO | 稀HNO3 | 铜屑 | H2O |
| D | Cl2 | 浓盐酸 | 高锰酸钾 | NaOH溶液 |
| A、A | B、B | C、C | D、D |
容量瓶上需标有以下6项中的( )
①温度 ②浓度 ③容量 ④压强 ⑤刻度线.
①温度 ②浓度 ③容量 ④压强 ⑤刻度线.
| A、①③⑤ | B、③⑤⑥ |
| C、①②④ | D、②④⑥ |